Stå opp
Iver Strandheim, Paul Andreas Aasen, Børge Sivertsen, Ragnhild Bang Nes, Trude Backer Mortensen, Siri Mathiassen & Emilie Føyen With
-
Iver Strandheim
psykologspesialist, Norges Fotballforbund
-
Paul Andreas Aasen
psykolog, Oslo kommune
-
Børge Sivertsen
seniorforsker ved Folkehelseinstituttet; professor II ved Institutt for psykisk helse, NTNU; forsker II ved Avdeling for forsking og innovasjon, Helse Fonna
-
Ragnhild Bang Nes
seniorforsker ved Folkehelseinstituttet; førsteamanuensis II ved PROMENTA, Psykologisk institutt, Universitetet i Oslo (UiO)
-
Trude Backer Mortensen
klinisk ernæringsfysiolog, Nordre Follo kommune
-
Siri Mathiassen
frisklivsveileder, Nordre Follo kommune
-
Emilie Føyen With
frisklivsveileder, Nordre Follo kommune
Context and objective: Insomnia is highly prevalent in the Norwegian adult population. Effective non-pharmacological treatment exists but is not available to the large majority of those suffering from insomnia. The aim of this study was to evaluate the effect of Get Up, a group-based intervention for insomnia based on cognitive behavioural therapy (CBT-I) and developed for easy implementation in community health care services in Norway.
Design and Setting: A randomized controlled trial study was conducted in Oppegård, Norway. Participants were randomly assigned to an active treatment condition (CBT-I) or to a wait list control condition, with participants in the latter condition receiving treatment after 5 months. The primary outcome measure was the Insomnia Severity Index (ISI), while secondary outcome measures included the PHQ-9 and GAD-7 instruments, measuring symptoms of depression and anxiety, respectively.
Main outcome measures and results: The intention-to-treat mixed-model repeated-measures analysis revealed that the treatment group had better short-term outcomes as measured by ISI compared to the control group.
Significantly reduced insomnia symptoms were observed in the treatment group (n = 16) compared to the wait list controls (n = 17), Cohen’s dbetween = 3,53. At five months follow up, participants in the treatment group had maintained their low ISI scores. Similar trends were also observed for symptoms of anxiety and depression.
Conclusions: The findings suggest that the community-based intervention Get Up may be a useful intervention for short and long-term management of insomnia, leading to substantial improvements of both insomnia severity and daytime emotional functioning. Limitations concerning the sample size means that care should be taken when generalizing the findings to the whole population.
Key words: insomnia, group therapy, sleep restriction therapy, CBT-I, Get Up, ISI.
Gruppebehandling for insomni kan være en god måte å møte etterspørselen av søvnbehandling i kommunen. Denne studien validerer effekten av det gruppebaserte behandlingsprogrammet Stå opp for insomni.
Insomni er vanlig. Mellom 8 og 15 prosent av den norske befolkningen oppfyller kriteriene for kronisk insomni (Pallesen, Sivertsen, Nordhus & Bjorvatn, 2014; Uhlig, Sand, Ødegård & Hagen, 2014). Insomni er dermed en av våre mest utbredte og undervurderte folkehelseutfordringer (Major et al., 2011), med store samfunnsøkonomiske og helsemessige følger for befolkningen (Daley, Morin, LeBlanc, Grégoire & Savard, 2009). Insomni er forbundet med økt risiko for å utvikle angstlidelser og depresjon (Baglioni et al., 2011; Chang, Ford, Mead, Cooper-Patrick & Klag, 1997; Neckelmann, Mykletun & Dahl, 2007), nedsatt stressmestring, redusert livskvalitet og sterkt forhøyet risiko for sykemelding og uføretrygd (Léger et al., 2012; Morin, Rodrigue & Ivers, 2003; Sivertsen et al., 2006). Flere rapporter fra Folkehelseinstituttet de senere årene har understreket viktigheten av å utvikle og teste programmer for å forebygge søvnproblemer som et sentralt grep for å for å bedre den psykiske helsen i befolkningen (Helse- og omsorgsdepartementet, 2019).
Interessekonflikter
Første- og andreforfatter har utviklet behandlingsmetoden og -materiellet, og tilbyr opplæring i Stå Opp-metoden til andre fagutøvere.
Behandlingsformer
I Norge kan vi hovedsakelig dele inn de tilgjengelige behandlingstilbudene for insomni i tre grupper. Disse inkluderer i) medikamentell behandling (hypnotika) hos fastlegen, ii) søvnkurs (psykoedukasjon) i regi av frisklivssentraler og iii) kognitiv atferdsterapi for insomni (CBT-I). Det er stor variasjon både innenfor og mellom de enkelte tilbudene både med tanke på hvordan behandlingen gjennomføres, og hvilken behandling som tilbys.
Hypnotika. En stor andel av dem som går til fastlegen med sine søvnvansker, får utskrevet sovemedisiner, også kalt hypnotika (Bjorvatn, Meland, Flo & Mildestvedt, 2017). Hypnotika regnes som en effektiv behandling for akutt søvnløshet (Buscemi et al., 2007), men anbefales ikke som behandling for kronisk insomni på grunn av risiko for bivirkninger, toleranseutvikling og misbruksfare (National Institutes of Health, 2009).
Sov Godt-kurs. Et annet tiltak for insomni og søvnvansker er Helsedirektoratets Sov Godt-kurs, som tilbys ved mange frisklivssentraler i norske kommuner. Dette er et rent psykoedukativt kurs over fire samlinger. Kurset inneholder undervisning om søvn, søvnvansker og ulike holdninger til søvn og informerer om prinsippene bak stimuluskontroll og søvnrestriksjon (Helsedirektoratet, 2016). Det finnes imidlertid ingen evaluering av dette kurset, og studier har funnet at psykoedukasjon i seg selv har liten effekt på insomni hvis den ikke kombineres med atferdsintervensjoner (Morin et al., 2006; Taylor, Schmidt-Nowara, Jessop & Ahearn, 2010).
CBT-I. Den behandlingsformen som derimot har vist seg å både være effektiv og som er det foretrukne behandlingsalternativet for kronisk insomni, er kognitiv atferdsterapi for insomni (CBT-I) (van Straten et al., 2018; Qaseem et al., 2016). CBT-I er en multi-komponent-behandling med innslag av psykoedukasjon om søvn, søvnhygieniske råd, avslapningsteknikker, kognitive teknikker og atferdsintervensjonene stimuluskontroll og søvnrestriksjon (Lichstein, Vander Wal & Dillon, 2012).
Det finnes ulike tilbydere av CBT-I-behandling i Norge, som Rask psykisk helsehjelp (RPH), internettbaserte behandlingsprogrammer og både private og offentlige søvnsentre. RPH er kommunale lavterskeltilbud som skal gi rask og effektiv hjelp for angst, depresjon og søvnvansker. Per mars 2019 hadde 55 kommuner og bydeler fått tilskudd til opprettelse av dette lavterskeltilbudet. Terapeutene i RPH mottar opplæring i CBT-I. En studie av Smith, Alves og Knapstad (2016) basert på data fra de tolv første kommunene som implementerte RPH, viste at 40,8 % av de som kontaktet RPH, rapporterte søvnproblemer. Ved avslutning av behandling oppga 44,5 % av disse at de ikke lenger hadde søvnproblemer, med noe variasjon mellom de enkelte kommunene.
De siste årene har det også blitt forsket på CBT-I-behandling ved hjelp av internett, blant annet internettverktøyet Sleep Healthy Using the Internet (SHUTi). En norsk studie av SHUTi har vist gode resultater for deltakere som gjennomførte behandlingen, men man fant også at 38 % falt fra i løpet av behandlingen (Hagatun et al., 2017). I tillegg til RPH og internettbaserte program finnes det noen få søvnklinikker i offentlig og privat regi som tilbyr CBT-I. Det samlede tilbudet på CBT-I i Norge er likevel ikke tilpasset den høye forekomsten av insomni. Det betyr at mange ikke har tilgang på den behandlingsformen med best evidens.
Formålet med studien
Insomni er dermed en av våre mest utbredte og undervurderte folkehelseutfordringer
Formålet med denne studien er å presentere og undersøke effekt av en gruppebasert behandlingsmetode for insomni i norske kommuner. CBT-I som gruppebehandling er anerkjent som like effektivt som individualbehandling (McCrae, Dautovich & Dzierzewski, 2010; Verbeek, Konings, Aldenkamp, Declerck & Klip, 2006). Oss bekjent har det ikke vært gjennomført effektstudier av gruppebehandling med CBT-I i Norge. Vi ønsket derfor å utvikle og teste en enkel CBT-I-modell som gruppebehandling i kommunehelsetjenesten. Vi kalte denne Stå Opp, siden det fokuseres særlig på atferdskomponentene søvnrestriksjon og stimuluskontroll. Valget om å fokusere mer på søvnrestriksjon og stimuluskontroll er basert på forskningen til Fernando III, Arroll og Falloon (2013), Blom og kolleger (2015) og Fallon og kolleger (2015), som har vist at et forenklet søvnbehandlingsopplegg med søvnrestriksjon gir gode resultater for pasienter med insomni. Problemstillingen i denne studien var om deltakelse i søvnbehandlingsgruppen Stå Opp var mer effektivt for insomnisymptomer enn det å stå på venteliste. I tillegg ønsket vi å undersøke om behandlingen var assosiert med bedring av deltakernes psykiske helse, i form av reduksjon av symptomer på angst og depresjon slik blant andre Hagatun og kolleger (2018), Manber og kolleger (2008) og Manber og kolleger (2011) tidligere har vist.
Metode
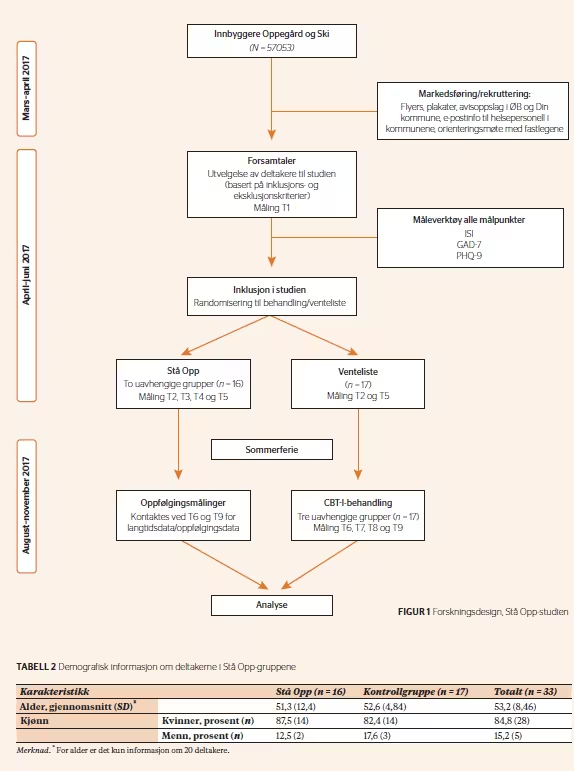
Rekruttering
Deltakerne ble rekruttert fra kommunene Oppegård og Ski i mars og april 2017. Det ble delt ut informasjonsmateriell om studien i begge kommunene. I tillegg ble det formidlet informasjon på kommunenes nettsider og i lokalavisen. Interesserte deltakere tok kontakt via telefon (n = 61), og 47 møtte til en forsamtale. For å inkluderes i selve studien måtte man: 1) være 18 år eller eldre, 2) være innbygger i Ski eller Oppegård kommune, 3) ha en skåre ≥ 15 på spørreskjemaet Insomnia Severity Index og 4) være motivert for behandling. Eksklusjonskriterier var bipolar lidelse, epilepsi, alvorlig depressiv episode, psykoselidelser, alvorlige personlighetsforstyrrelser, døgnrytmeforstyrrelse og andre søvnsykdommer der CBT-I er kontraindisert (søvnapné, narkolepsi, parasomnier og Restless Legs Syndrome). Dette ble kartlagt og vurdert i forsamtalen av psykolog med direkte spørsmål om symptomer på disse lidelsene.
Utvalg
Av de 61 som ble invitert til forsamtalen, var det 28 (46 %) som ikke ble inkludert i studien, enten fordi de ikke møtte opp til forsamtalene (n = 14), uttrykte at de ikke var motiverte for behandling etter å ha fått skissert behandlingsforløpet (n = 5), ikke kunne delta på grunn av praktiske forhold (n = 2), hadde alvorlig psykisk lidelse (n = 4), hadde kommunikasjonsvansker som gjorde gruppebehandling vanskelig (n = 2), eller hadde en døgnrytmeforstyrrelse som krevde annen type behandling (n = 1). Pasienter som oppfylte inklusjonskriteriene, og som ønsket å delta i studien (n = 33), signerte et samtykkeskjema og ble randomisert til en intervensjonsgruppe (n = 16) eller en venteliste/kontrollgruppe (n = 17). Det endelige utvalget besto av 28 kvinner og 5 menn. Én deltaker i intervensjonsgruppen avbrøt behandlingen etter første gruppesamling på grunn av praktiske forhold.
Deltakerne ble randomisert før forsamtalene på bakgrunn av når de meldte sin interesse for studien/behandlingen. Denne listen ble laget fortløpende, slik at nummer 1 på listen meldte sin interesse først, og nummer 61 henvendte seg sist. Deltakere med oddetall ble tilbudt behandling i mai–juni 2017, mens deltakere med partall fikk tilbud om å stå på venteliste frem til behandlingsstart i september samme år.
Deltakerne i intervensjonsgruppen fylte ut spørreskjemaene i etterkant av gruppesamling 2, 3, 5 og 7, heretter kalt T2, T3, T4 og T5 (se figur 1). Deltakerne som sto på venteliste, fylte ut spørreskjema ved måletidspunkt T2 og T5, før de fikk behandling høsten 2017. De fylte da ut spørreskjemaene etter gruppesamling 1, 3, 5 og 7 (som var ved avsluttet behandling), heretter kalt T6, T7, T8, T9. Deltakerne i intervensjonsgruppen fylte også ut spørreskjema ved T6 og T9 (to og fem måneder etter avsluttet behandling).
Intervensjon
Stå Opp legger vekt på de atferdsterapeutiske elementene i CBT-I, og da særlig søvnrestriksjon
Stå Opp er en gruppebasert behandling basert på CBT-I utviklet i Oppegård kommune, og er nærmere beskrevet i Behandlingsmanual for Stå Opp (Aasen & Strandheim, 2019). Stå Opp innebærer sju samlinger på 90 minutter over ni uker (se tabell 1). Det var åtte deltakere i hver gruppe. Disse gjennomførte søvnrestriksjon og stimuluskontroll etter å ha mottatt enkel psykoedukasjon om søvn. Deltakerne fylte ut ei søvndagbok. Søvndagboka brukes til å kartlegge den subjektive opplevelsen av søvnkvalitet og søvnlengde. Den er i tillegg grunnlaget for å regne ut søvneffektiviteten, som refererer til hvor stor andel av tiden tilbrakt i senga deltakeren sover. Søvnrestriksjonen gjennomføres med utgangspunkt i gjennomsnittlig rapportert søvnlengde i søvndagboka. I tillegg benyttes søvneffektivitet som grunnlag for å fremskynde eller utsette leggetidspunkt underveis i behandlingen. Det var totalt fire behandlere. Disse inkluderte en klinisk ernæringsfysiolog og en fysioterapeut ansatt ved Frisklivssentralen, en kommunepsykolog (Oppegård kommune) og en psykologistudent (UiO). Kommunepsykologen deltok i alle gruppene og sørget for at behandlingen i alle gruppene lå tett opp mot behandlingsmanualen.

TABELL 1. Oversikt over innholdet i de ulike gruppesamlingene i Stå Opp
Stå Opp legger vekt på de atferdsterapeutiske elementene i CBT-I, og da særlig søvnrestriksjon. Behandlingen har mindre fokus på søvnhygiene enn ordinær CBT-I-behandling og inneholder ikke avslapningstrening og kognitive teknikker. Ved de første gruppesamlingene benyttes elementer fra Motiverende intervju dersom deltakere er usikre på om de er i stand å gjennomføre behandlingen (Rollnick & Miller, 1995). Det er spesielt ansvarliggjøring og å rulle med motstanden som benyttes i møte med deltakeres ambivalens. Å rulle med motstanden innebærer å understreke deltakerens valg, kontroll og autonomi. Deltakernes feilaktige antakelser rundt søvn utforskes gjennom samtaler i gruppa. Når deltakerne opplever bedret søvnkvalitet som følge av atferdsendringen, endres ofte også tidligere feilantakelser de har hatt rundt søvn. Denne endringen blir igjen forsterket ved at erfaringene deles og diskuteres i gruppa.
Instrumenter
Primærmål. Insomnia Severity Index (ISI) er et mye brukt spørreskjema som kartlegger alvorlighetsgraden av pasientens søvnplager. ISI har vist seg å være et valid mål på insomni (Morin, Belleville, Bélanger, & Ivers, 2011). ISI består av 7 ledd som ber pasienten rangere sine plager ved hjelp av fem svaralternativer fra 0 («ingen plager») til 4 («veldig store plager»). Alvorlighetsgrad av insomni grupperes på bakgrunn av sumskåren (0–28), der 0–7 indikerer «Ingen klinisk signifikant insomni», 8–14 «Subterskel insomni», 15–21 «Klinisk insomni (moderat)» og 22–28 «Klinisk insomni (alvorlig)». En sumskåre på 15 eller mer ble benyttet som inklusjonskriterium for deltakelse i vår studie. ISI har vist seg å være sensitiv for endring, og er dermed egnet for å måle bedring både under og i etterkant av behandling. Morin og kolleger klassifiserte i sin studie fra 2011 en reduksjon i ISI-skåre på 4,65 som «mild bedring», 8,36 som «moderat bedring» og 9,89 som «markant bedring» (Morin et al., 2011).
Sekundærmål. Symptomer på angst og depresjon ble målt med spørreskjemaene GAD-7 (the 7-item Generalized Anxiety Disorder Scale) og PHQ-9 (Patient Health Questionnaire Mood Scale), som begge har vist seg å være valide og godt utprøvde instrumenter for å kartlegge psykisk helse (Kroenke, Spitzer & Williams, 2001; Löwe et al., 2008; Martin, Rief, Klaiberg & Braehler, 2006; Spitzer, Kroenke, Williams & Löwe, 2006). GAD-7 består av 7 ledd med svaralternativer fra 0 til 3 som gir en total sumskåre på 0–21. En sumskåre på 10 eller høyere indikerer et klinisk nivå av generalisert angst (Löwe et al., 2008). PHQ-9 består av 9 ledd som måler hyppigheten av ulike depresjonssymptomer i løpet av de siste to ukene (skåres fra 0 til 3). Sumskåren går fra 0 til 27, og en skåre på 9 eller mer gir indikasjon på klinisk depresjon (Kroenke, Spitzer, Williams, & Löwe, 2010, Manea, Gilbody, & McMillan, 2012). Ettersom PHQ-9 inneholder to ledd som spør om søvn og tretthet, konstruerte vi en versjon av PHQ-9 som utelot disse to leddene. Dette ble gjort for å se om søvnbehandlingen også har effekt på andre aspekter ved depresjon.
Den interne konsistensen på spørreskjemaene ble beregnet ved hjelp av Cronbachs alfa, og var før behandling og ved fullført behandling på henholdsvis .54 og .95 (ISI), .77 og .91 (GAD-7), og .66 og .90 (PHQ-9).
For å vurdere den kliniske effekten av behandlingen tok vi utgangspunkt i det Morin og kolleger (2009) definerer som at deltakerne responderer på behandling (responders) og oppnår remisjon (remitters). De som responderer på behandling, er deltakerne som oppnår en reduksjon i sumskåren på ISI på mer enn 7 poeng sammenlignet med baseline. Remisjon betegner en sumskåre på ISI som er mindre enn 8 etter behandling (ingen klinisk signifikant insomni). Deltakere med manglende data fikk videreført sin status fra forrige observasjon, og dermed ble deltakere som kun hadde data ved oppstart, men som falt fra under behandlingen, definert som ikke-responderende eller ikke oppnådd remisjon ved alle målepunkter.
Statistiske analyser
Analysene ble gjennomført ved hjelp av IBM© SPSS Statistics, versjon 25. Det ble først gjennomført t-tester som viste effekt av intervensjonen. Mauchly’s Test of Sphericity viste at antakelsen om sfærisitet var brutt, og antakelsene som ligger til grunn for lineære analyser, ble møtt. Vi analyserte derfor dataene ved hjelp av linear mixed model for repeated-measures-analyser (LMM). Alle de 33 deltakerne som startet i behandling, ble inkludert i analysene – også deltakeren som falt fra etter én gruppesamling. Manglende verdier i datasettet ble estimert ved hjelp av restricted maximum likelihood (REML).
Studien er en randomisert kontrollert studie med pre- og post-målinger, i tillegg til en måling etter fem måneder.
Sumskårene på ISI, GAD-7 og PHQ-9 ble brukt som avhengige variabler, og gruppe (intervensjon/kontroll) og måletidspunkt som uavhengige variabler. LMM ble gjennomført med en ustrukturert kovariansstruktur (UN). I analysen av mellomgruppeeffekter ble tid (fem tidspunkter for begge grupper) og gruppe (intervensjon/kontroll) inkludert i modellen sammen med et interaksjonsledd (tid x gruppe). For å undersøke om kontrollgruppen hadde effekt av behandling, ble det i tillegg gjennomført LMM-analyser, der vi undersøkte om det var en effekt av behandling også for denne gruppen.
For å gjennomføre en Pearsons kjikvadrat-test definerte vi de to betingelsene insomni og ikke-insomni. Ikke-insomni ble definert som å være under klinisk kuttskåre på utfallsmålet ISI (sumskåre ISI < 15). Det ble i tillegg kjørt en analyse der remisjon tilsvarte en sumskåre på ISI < 8, som i ISI kategoriseres som ingen klinisk signifikant insomni.
Effektstørrelsene med konfidensintervaller ble beregnet som Cohens d, som beskrevet i Coe (2002), for både innengruppe- og mellomgruppeeffekter. Utregningene ble gjort med Effect Size Calculator (Centre For Evaluation and Monitoring at Durham University, 2006). I denne artikkelen benevnes effekter mellom intervensjons- og kontrollgruppen som Cohens dbetween. Der vi sammenligner skårer ved to ulike måletidspunkter innenfor samme gruppe, benevnes dette som Cohens dwithin. Effektstørrelser i Cohens d klassifiseres som liten (0,2), moderat (0,5) og stor (0,8).
Meta-analyser av CBT-I har rapportert effektstørrelser for totalskåre på ISI som Cohens d over 0,9 (Okajima, Komada & Inoue, 2011; van Straten et al., 2018). Kontrollgrupper basert på ventelister har trolig liten effekt (Morin et al., 2006; Taylor, Schmidt-Nowara, Jessop & Ahearn, 2010). Med utgangspunkt i en forventet mellom-gruppe-effektstørrelse på ISI på 1,0 vil det være tilstrekkelig med 17 pasienter i hver gruppe, gitt en statistisk styrke på 0,80, alfa-verdi på 0,05 (to-halet test).
Etikk
Studien er godkjent av Regional etisk komité for medisinsk og helsefaglig forskning, Sør-Øst (2017/462), og utfallsmål er forhåndsregistrert hos https://clinicaltrials.gov/ (NCT03177967). Deltakerne signerte samtykkeerklæring og kunne fritt trekke seg, uten å oppgi grunn, når som helst i studien. Ferdig utfylte spørreskjemaer og kodenøkkel med personinformasjon ble lagret separat.
Resultatene tyder på at intervensjonen har god effekt på insomni
Resultater
Utvalget besto av 33 deltakere (28 kvinner og 5 menn) med gjennomsnittsalder på 53,2 år ved inklusjon i studien. Det var ingen signifikante forskjeller (p > 0,05) mellom intervensjons- og kontrollgruppen i alder, kjønn eller på noen av måleinstrumentene (ISI, PHQ-9, GAD-7) ved T1. Kjønns- og aldersfordeling er presentert i tabell 2.
Behandlingseffekt for insomni
I intervensjonsgruppen var det en signifikant reduksjon (p < 0,001) i skårene på ISI fra forsamtale (T1) til endt behandling (T5) basert på LMM-analysen av innengruppeeffekten. Det var en gjennomsnittlig reduksjon i ISI-skåre for denne gruppen på 16,02 (se tabell 3). Mellomgruppeeffekten ble estimert til Cohens dbetween = 3,53. Det var her en signifikant interaksjonseffekt av gruppe × tid (p < 0,001) fra T1 til T5 (LMM-analyse). Dette tyder på at intervensjonen har hatt effekt på insomnisymptomene.
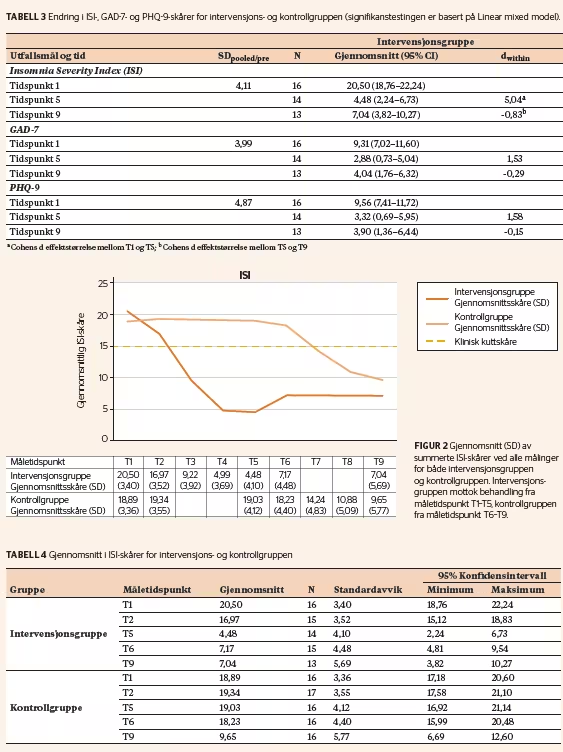
Figur 2 viser sumskårene på ISI for intervensjons- og kontrollgruppen over tid. Måletidspunkt T1 er ved forsamtale. T2 er etter én ukes behandling, og T5 er ved avslutning av behandling for intervensjonsgruppen. T6 er ved oppstart av behandling for ventelistegruppen og er samtidig to måneders oppfølging for intervensjonsgruppen. Måletidspunkt T9 er ved avslutning av behandling for ventelistegruppen. Dette tilsvarer også fem måneders oppfølging for intervensjonsgruppen. Som vi ser av figuren, er det en nedgang i insomnisymptomer under gruppebehandlingen hos deltakerne i intervensjonsgruppen, mens kontrollgruppen har et stabilt symptomnivå fram til oppstart av behandling ved T6. Etter endt behandling for gruppen som sto på venteliste, ser vi ved en LMM innengruppeanalyse en signifikant reduksjon (p < 0,001) i insomniplager (ISI) fra forsamtale (T1) til endt behandling (T9; se tabell 3).
I tråd med figur 2 var det en signifikant reduksjon i insomnisymptomer i intervensjonsgruppen fra T2– [KH1] T4 (p < 0,001). Økningen i symptomer i intervensjonsgruppen mellom T5 og T6 er også statistisk signifikant (p < 0,01). For kontrollgruppen er det kun en signifikant reduksjon i symptomer (p < 0,001) etter oppstart av behandling, mellom T6 og T7, og mellom T7 og T8 (p < 0,01). Etter endt behandling er gjennomsnittsskåren for hver av gruppene under den kliniske kuttskåren (sumskåre ISI < 15). For utvalget som helhet observerte vi en gjennomsnittlig reduksjon i ISI-skåre > 9,89, som klassifiseres som markant i henhold til Morin og kolleger (2011).
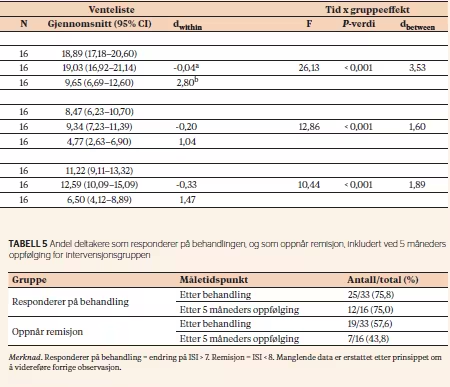
Pearsons kjikvadrat-test viste en statistisk signifikant forskjell mellom gruppene ved måletidspunkt T5, både ved en kuttskåre på 15 (χ2 = 25,9, df = 1, p < 0,001) og ved en kuttskåre på 8 (χ2 = 19,2, df = 1, p < 0,001).
Behandlingseffekt på angst- og depresjonssymptomer
I tillegg til reduksjon i symptomer på insomni så vi også en reduksjon i selvrapporterte angst- og depresjonssymptomer. Da vi sammenlignet intervensjonsgruppen med kontrollgruppen ved hjelp av LMM-analyser, var det en signifikant interaksjonseffekt av gruppe × tid (p < 0,001) fra T1 til T5 på både GAD-7 og PHQ-9, med en mellomgruppeeffekt for GAD-7 på Cohens dbetween = 1,60, og dbetween = 1,89 for PHQ-9. Dette tyder på at intervensjonen har effekt på både angst- og depresjonssymptomene.
Figur 3 viser sumskårene på PHQ-9 for intervensjons- og kontrollgruppen over tid. Som vi ser av figuren, er det en nedgang i depresjonssymptomer under gruppebehandlingen hos deltakerne i intervensjonsgruppen, mens kontrollgruppen har et stabilt nivå fra T2 og fram til oppstart av behandling ved T6.
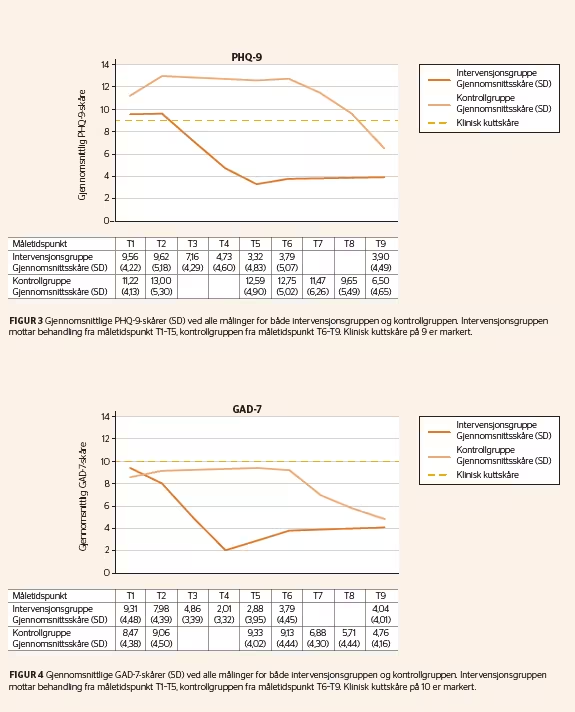
Figur 4 viser sumskårene på GAD-7 for intervensjons- og kontrollgruppen over tid. Som vi ser av figuren, er det en nedgang i angstsymptomer under gruppebehandlingen hos deltakerne i intervensjonsgruppen, mens kontrollgruppen har et stabilt nivå på symptomene fram til deres oppstart av behandling ved T6. Ved oppstart hadde begge gruppene i gjennomsnitt nivåer på GAD-7 under klinisk kuttskåre (sumskåre < 10), og reduksjonen må tolkes med dette i tankene.
Diskusjon
Formålet med denne studien var å presentere og evaluere effekt av søvnintervensjonen Stå Opp, en CBT-I-basert gruppeintervensjon for insomni. Resultatene tyder på at intervensjonen har god effekt på insomni og assosierte angst- og depresjonssymptomer. Vi observerte en signifikant nedgang i ISI-skåre for intervensjonsgruppen sammenlignet med kontrollgruppen, og mellomgruppeeffekten var stor. Dette er i tråd med van Straten og kollegers (2018) metaanalyse, som rapporterer store mellomgruppeeffekter av behandling for insomni. Vi fant også en stor innengruppeeffekt av behandlingen for insomni, og dette er i tråd med resultatene fra forskning på CBT-I både som gruppe- og individuell behandling utført av Blom et al. (2015) og Davidson et al. (2017). Blom og kolleger fokuserte i likhet med Stå Opp på stimuluskontroll og søvnrestriksjon i CBT-I-behandlingen. Den svenske studien er i så måte en studie som kan sammenlignes med vår, også i form av relativt like inklusjons- og eksklusjonskriterier. Dette tyder på at også Stå Opp er en effektiv metode for å behandle insomni.
Klinisk relevans
Insomni er et betydelig folkehelseproblem med store konsekvenser for både enkeltmennesker og for samfunnet som helhet. Denne studien viser at Stå Opp-grupper som behandlingsform kan ha en betydelig behandlingseffekt. Ettersom behandlingsopplegget i hovedsak fokuserer på atferdskomponentene i CBT-I, kreves relativt lite ressurser og forkunnskap for å sette i gang søvnbehandlingsgrupper etter Stå Opp-metoden. På tross av dette viser vår studie at effektstørrelsene ikke står tilbake for resultatene fra forskning på mer omfattende gruppebasert CBT-I-behandling (Davidson et al., 2017; Koffel, Koffel & Gehrman, 2015. Samlet sett fremstår dette som gode argumenter for å tilby en forenklet søvnbehandlingsmodell i gruppeformat i norske kommuner.
Mange frisklivsansatte har allerede god kunnskap om de virksomme elementene i søvnbehandling gjennom Sov Godt-opplæringen. Det er derfor trolig en nyttig plattform for å videreutvikle tilbudet i frisklivssentralene til et behandlingsopplegg i tråd med Stå Opp-metodikken. Terapeuter i Rask psykisk helsehjelp har fått en innføring i CBT-I-behandling gjennom utdanning levert av Norsk forening for kognitiv terapi, og skal kunne tilby denne behandlingen. Basert på våre resultater og kunnskapen om hvor krevende det er å implementere nye behandlingsprogrammer (Joyce og Showers, 2002), tror vi at opplæring i en forenklet, men effektiv gruppebehandling som Stå Opp vil kunne bedre både tilgjengeligheten og effekten av søvnbehandling som gis i RPH-kommuner. Vi har utarbeidet en behandlingsmanual, deltakerhefter og annet undervisningsmateriell som kan distribueres til kommuner som ønsker å prøve behandlingsopplegget.
Begrensninger og videre forskning
Studien vår har relativt få deltakere, og det er derfor behov for replikasjon i et større utvalg. Som følge av praktiske forhold var det heller ikke mulig å få til langtidsoppfølging for kontrollgruppen, noe som er en svakhet ved studien. Deltakerne benyttet søvndagbok i behandlingen, men vi har ikke sett på søvnlengde som et eget utfallsmål. Dette ville gjort det lettere å sammenligne våre resultater med andre behandlingsstudier på insomni.
I utgangspunktet ønsket vi også å sammenligne Stå Opp med standard kommunal oppfølging (Sov Godt), men dessverre lyktes vi ikke med å rekruttere nok deltakere til sistnevnte betingelse. Fremtidig forskning bør sikte mot å benytte aktive kontrollgrupper når effekten av ulike CBT-I intervensjoner skal evalueres. Design som også muliggjør å undersøke en potensiell forebyggende effekt med tanke på angst- og depresjonsplager, er likeledes ønskelig. Fremtidige studier bør også sammenligne Stå Opp-behandling med andre former for søvnbehandling. Stå Opp-tilnærmingen er noe mer ressurskrevende enn både Sov Godt-kurset og internettbaserte tilnærminger og bør følgelig gi større effekt for å prioriteres i kommunehelsetjenesten. Dette kan være tilfellet. Det er også relevant å se våre resultater i lys av en «stepped care»-tankegang, som mange kommuner benytter i sine psykisk helsetjenester. Fremtidig forskning bør forsøke å undersøke om Stå Opp kan være et kostnadseffektivt «første trappetrinn» i omsorgstrappen når man søker hjelp for insomni, fremfor oppfølging hos fastlege, individualterapeut i RPH eller gjennom Sov Godt-kurs. Vi mener vår studie peker i retning av at det kan være tilfellet. Andre viktige områder for utforskning er hvem Stå Opp ikke fungerer for, hvem som foretrekker andre behandlingsformer, og hvordan vi kan bygge opp et likeverdig behandlingstilbud for hele populasjonen med insomni, med de behandlingsformene som eksisterer.
Konklusjon
Denne studien validerer effekten av Stå Opp for insomni, og viser også god effekt på depresjons- og angstsymptomer. Til tross for enkelte metodiske svakheter gir resultatene grunn til optimisme med tanke på gjennomføring av gruppebasert insomnibehandling med Stå Opp i kommunehelsetjenesten. Behandlingsmodellen bygger på kjente søvnbehandlingsprinsipper, tilpasset for enkel implementering i kommunehelsetjenesten, slik at man kan møte etterspørselen av søvnbehandling på en effektiv måte.
Referanser
Aasen, P.A., & Strandheim, I. (2019). Behandlingsmanual for Stå Opp: Søvnbehandling utviklet i Oppegård kommune. Oppegård: U.f.
Baglioni, C., Battagliese, G., Feige, B., Spiegelhalder, K., Nissen, C., Voderholzer, U., . . . Riemann, D. (2011). Insomnia as a predictor of depression: A meta-analytic evaluation of longitudinal epidemiological studies. Journal of Affective Disorders, 135(1), 10 - 19. https://doi.org/10.1016/j.jad.2011.01.011
Blom, K., Tarkian Tillgren, H., Wiklund, T., Danlycke, E., Forssén, M., Söderström, A., . . . Kaldo, V. (2015). Internet-vs. group-delivered cognitive behavior therapy for insomnia: A randomized controlled non-inferiority trial. Behaviour Research and Therapy, 70, 47 - 55. https://doi.org/10.1016/j.brat.2015.05.002
Bjorvatn, B., Meland, E., Flo, E., & Mildestvedt, T. (2017). High prevalence of insomnia and hypnotic use in patients visiting their general practitioner. Family Practice, 34(1), 20 - 24. https://doi.org/10.1093/fampra/cmw107
Buscemi, N., Vandermeer, B., Friesen, C., Bialy, L., Tubman, M., Ospina, M., . . . Witmans, M. (2007). The efficacy and safety of drug treatments for chronic insomnia in adults: A meta-analysis of RCTs. Journal of General Internal Medicine, 22(9), 1335 - 1350. https://doi.org/10.1007/s11606-007-0251-z
Chang, P.P., Ford, D.E., Mead, L.A., Cooper-Patrick, L., & Klag, M.J. (1997). Insomnia in young men and subsequent depression: The Johns Hopkins precursors study. American Journal of Epidemiology, 146(2), 105 - 114. https://doi.org/10.1093/oxfordjournals.aje.a009241
Coe, R. (2002). It’s the effect size, stupid: What effect size is and why it is important. Paper presentert ved Annual Conference of the British Educational Research Association, University of Exeter, England.
Daley, M., Morin, C.M., LeBlanc, M., Grégoire, J.-P., & Savard, J. (2009). The economic burden of insomnia: Direct and indirect costs for individuals with insomnia syndrome, insomnia symptoms, and good sleepers. Sleep, 32(1), 55 - 64. https://doi.org/10.1016/S1073-5437(10)79480-8
Davidson, J.R., Dawson, S., & Krsmanovic, A. (2017). Effectiveness of group cognitive behavioral therapy for insomnia (CBT-I) in a primary care setting. Behavioral Sleep Medicine, 1 - 13. https://doi.org/10.1080/15402002.2017.1318753
Falloon, K., Elley, C.R., Fernando, A., Lee, C.A., Arrol, B. (2015). Simplified sleep restriction for insomnia in general practice: a randomised controlled trial. British Journal of General Practice, 65 (637), e508-e515. https://doi.org/10.3399/bjgp15X686137
Fernando III, A., Arroll, B., & Falloon, K. (2013). A double-blind randomised controlled study of a brief intervention of bedtime restriction for adult patients with primary insomnia. Journal of Primary Health Care, 5(1), 5 - 10. https://doi.org/10.1071/HC13005
Hagatun, S., Vedaa, Ø., Nordgreen, T., Smith, O.R.F., Pallesen, S., Havik, O.E., . . . Sivertsen, B. (2017). The short-term efficacy of an unguided internet-based cognitive-behavioral therapy for insomnia: A randomized controlled trial with a six-month nonrandomized follow-up. Behavioral Sleep Medicine, 1 - 23. https://doi.org/10.1080/15402002.2017.1301941
Hagatun, S., Vedaa, Ø., Harvey, A.G., Nordgreen, T., Smith, O., Pallesen, S., … Sivertsen, B. (2018). Internet-delivered cognitive-behavioral therapy for insomnia and comorbid symptoms. Internet interventions, 12, 11–15. https://doi.org/10.1016/j.invent.2018.02.003
Helsedirektoratet. (2016). Sov godt: Mal for søvnkurs for deg som jobber på frisklivssentralen [elektronisk versjon] Hentet fra https://helsedirektoratet.no/publikasjoner/sov-godt-mal-for-sovnkurs-for...
Helse- og omsorgsdepartementet. (2019). Folkehelsemeldinga: Gode liv i eit trygt samfunn. (Meld. St. nr. 19 2018 - 2019). Hentet fra https://www.regjeringen.no/no/dokumenter/meld.-st.-19-20182019/id2639770/
Joyce, B.R., & Showers, B. (2002). Student achievement through staff development (3rd ed.). Alexandria, VA: Association for Supervision & Curriculum Deve (ASCD)
Koffel, E.A., Koffel, J.B., & Gehrman, P.R. (2015). A meta-analysis of group cognitive behavioral therapy for insomnia. Sleep medicine reviews, 19, 6 - 16. https://doi.org/10.1016/j.smrv.2014.05.001
Kroenke, K., Spitzer, R.L., & Williams, J.B.W. (2001). The PHQ-9: Validity of a Brief Depression Severity Measure. Journal of General Internal Medicine, 16(9), 606 - 613. https://doi.org/10.1046/j.1525-1497.2001.016009606.x
Kroenke, K., Spitzer, R.L., & Williams, J.B.W., Löwe, B. (2010). The Patient Health Questionnaire Somatic, Anxiety, and Depressive Symptom Scales: a systematic review. General Hospital Psychiatry, 32(4), 345 - 359. https://doi.org/10.1016/j.genhosppsych.2010.03.006
Léger, D., Morin, C.M., Uchiyama, M., Hakimi, Z., Cure, S., & Walsh, J.K. (2012). Chronic insomnia, quality-of-life, and utility scores: Comparison with good sleepers in a cross-sectional international survey. Sleep Medicine, 13(1), 43 - 51. https://doi.org/10.1016/j.sleep.2011.03.020
Lichstein, K.L., Vander Wal, G.S., & Dillon, H.R. (2012). Insomnia III: Therapeutic approaches. I C.M. Morin & C.A. Espie (red.), The Oxford handbook of sleep and sleep disorders. Oxford: Oxford University Press. https://doi.org/10.1093/oxfordhb/9780195376203.013.0023
Löwe, B., Decker, O., Müller, S., Brähler, E., Schellberg, D., Herzog, W., & Herzberg, P.Y. (2008). Validation and standardization of the Generalized Anxiety Disorder Screener (GAD-7) in the general population. Medical Care, 46(3), 266 - 274. https://doi.org/10.1097/MLR.0b013e318160d093
Major, E., Dalgard, O., Mathisen, K., Nord, E., Ose, S., Rognerud, M., & Aarø, L. (2011). Bedre føre var ... Psykisk helse: Helsefremmende og forebyggende tiltak og anbefalinger. (2011: 1). Oslo: Nasjonalt folkehelseinstitutt. Lastet ned fra https://www.fhi.no/publ/2011/bedre-fore-var---psykisk-helse-hels/ den 08.02.2018.
Manber, R., Bernert, R.A., Suh, S., Nowakowski, S., Siebern, A.T., & Ong, J. C. (2011). CBT for insomnia in patients with high and low depressive symptom severity: adherence and clinical outcomes. Journal of Clinical Sleep Medicine, 7(6), 645 - 652. https://doi.org/10.5664/jcsm.1472
Manber, R., Edinger, J.D., Gress, J.L., Pedro-Salcedo, M.G.S., Kuo, T.F., & Kalista, T. (2008). Cognitive behavioral therapy for insomnia enhances depression outcome in patients with comorbid major depressive disorder and insomnia. Sleep, 31(4), 489 - 495. https://doi.org/10.1093/sleep/31.4.489
Manea, L., Gilbody, S., & McMillan, D. (2012). Optimal cut-off score for diagnosing depression with the Patient Health Questionnaire (PHQ-9): A meta-analysis. Canadian Medical Association Journal, 184(3), E191-E196. https://doi.org/10.1503/cmaj.110829
Martin, A., Rief, W., Klaiberg, A., & Braehler, E. (2006). Validity of the brief patient health questionnaire mood scale (PHQ-9) in the general population. General hospital psychiatry, 28(1), 71 - 77. https://doi.org/10.1016/j.genhosppsych.2005.07.003
McCrae, C.S., Dautovich, N.D., & Dzierzewski, J.M. (2010). Short-term and group treatment approaches [elektronisk versjon]. I M.J. Sateia, D.J. Buysse & M.J. Sateia (red.), Insomnia: diagnosis and treatment (s. 310 - 341). London: Informa Healthcare. https://doi.org/10.3109/9781420080803.028
Morin, C.M., Belleville, G., Bélanger, L., & Ivers, H. (2011). The insomnia severity index: Psychometric indicators to detect insomnia cases and evaluate treatment response. Sleep, 34(5), 601 - 608. https://doi.org/10.1093/sleep/34.5.601
Morin, C.M., Bootzin, R.R., Buysse, D.J., Edinger, J.D., Espie, C.A., & Lichstein, K.L. (2006). Psychological and behavioral treatment of insomnia: Update of the recent evidence (1998–2004). Sleep, 29(11), 1398 - 1414. https://doi.org/10.1093/sleep/29.11.1398
Morin, C.M., Rodrigue, S., & Ivers, H. (2003). Role of stress, arousal, and coping skills in primary insomnia. Psychosomatic Medicine, 65(2), 259 - 267. https://doi.org/10.1097/01.PSY.0000030391.09558.A3
Morin, C.M., Vallières, A., Guay, B., Ivers, H., Savard, J., Mérette, C., . . . Baillargeon, L. (2009). Cognitive Behavioral Therapy, Singly and Combined With Medication, for Persistent Insomnia: A Randomized Controlled Trial. Journal of the American Medical Association, 301(19), ss. 2005–2015. https://doi.org/10.1001/jama.2009.682
National Institutes of Health. (2009). NIH State-of-the-science conference statement on manifestations and management of chronic insomnia in adults. Focus, 7(4), 538 - 546. https://doi.org/10.1176/foc.7.4.foc538
Neckelmann, D., Mykletun, A., & Dahl, A.A. (2007). Chronic insomnia as a risk factor for developing anxiety and depression. Sleep, 30(7), 873 - 880. https://doi.org/10.1093/sleep/30.7.873
Okajima, I., Komada, Y., & Inoue, Y. (2011). A meta-analysis on the treatment effectiveness of cognitive behavioral therapy for primary insomnia. Sleep and Biological Rhythms, 9(1), 24 - 34. https://doi.org/10.1111/j.1479-8425.2010.00481.x
Pallesen, S., Sivertsen, B., Nordhus, I.H., & Bjorvatn, B. (2014). A 10-year trend of insomnia prevalence in the adult Norwegian population. Sleep Medicine, 15(2), 173 - 179. https://doi.org/10.1016/j.sleep.2013.10.009
Qaseem, A., Kansagara, D., Forciea, M., Cooke, M., & Denberg, T.D. (2016). Management of chronic insomnia disorder in adults: A clinical practice guideline from the American college of physicians. Annals of Internal Medicine, 165(2), 125 - 133. https://doi.org/10.7326/M15-2175
Rollnick, S., & Miller, W. (1995). What is Motivational Interviewing? Behavioural and Cognitive Psychotherapy, 23(4), 325 - 334. https://doi.org/10.1017/S135246580001643X
Sivertsen, B., Øverland, S., Neckelmann, D., Glozier, N., Krokstad, S., Pallesen, S., . . . Mykletun, A. (2006). The long-term effect of insomnia on work disability: the HUNT-2 historical cohort study. American Journal of Epidemiology, 163(11), 1018 - 1024. https://doi.org/10.1093/aje/kwj145
Smith, O.R., Alves, D.E. & Knapstad, M. (2016). Rask psykisk helsehjelp: Evaluering av de første 12 pilotene i Norge. Oslo: Folkehelseinstituttet.
Spitzer, R.L., Kroenke, K., Williams, J.B., & Löwe, B. (2006). A brief measure for assessing generalized anxiety disorder: The GAD-7. Archives of Internal Medicine, 166(10), 1092 - 1097. https://doi.org/10.1001/archinte.166.10.1092
Taylor, D.J., Schmidt-Nowara, W., Jessop, C.A., & Ahearn, J. (2010). Sleep restriction therapy and hypnotic withdrawal versus sleep hygiene education in hypnotic using patients with insomnia. Journal of Clinical Sleep Medicine, 6(2), 169 - 175. https://doi.org/10.5664/jcsm.27767
Uhlig, B.L., Sand, T., Ødegård, S.S., & Hagen, K. (2014). Prevalence and associated factors of DSM-V insomnia in Norway: the Nord-Trøndelag health study (HUNT 3). Sleep Medicine, 15(6), 708 - 713. https://doi.org/10.1016/j.sleep.2014.01.018
van Straten, A., van der Zweerde, T., Kleiboer, A., Cuijpers, P., Morin, C.M., & Lancee, J. (2018). Cognitive and behavioral therapies in the treatment of insomnia: A meta-analysis. Sleep Medicine Reviews, 38, 3 - 16. https://doi.org/10.1016/j.smrv.2017.02.001
Verbeek, I.H., Konings, G.M., Aldenkamp, A.P., Declerck, A.C., & Klip, E.C. (2006). Cognitive behavioral treatment in clinically referred chronic insomniacs: Group versus individual treatment. Behavioral Sleep Medicine, 4(3), 135 - 151. https://doi.org/10.1207/s15402010bsm0403_1
