Forsinket søvnfasesyndrom
Ståle Pallesen
-
Ståle Pallesen
Institutt for samfunnspsykologi, Universitetet i Bergen
staale.pallesen@psysp.uib.no
Delayed Sleep Phase Syndrome
Delayed sleep phase syndrome (DSPS) is a disorder in which the major sleep episode is delayed in relation to the desired clock time that results in difficulties falling asleep and/or difficulties in awakening at the desired time. Patients are not able to adjust their own circadian rhythm without some form of help. DSPS impairs social, educational and vocational performance. Although previous studies show that the prevalence of DSPS may vary, most would agree that the disorder is more common among children, adolescents and young adults. The disorder probably develops through an interplay of biological and behavioural factors. The biological factors probably involve some kind of anomalies in the intrinsic circadian oscillator whereas behaviours, such as staying up late during vacations and sleeping at daytime, are regarded as typically contributing factors to development of DSPS. Popular and effective interventions generally include light therapy and the administration of exogenous melatonin. Chronotherapy and sleep hygiene may also have beneficial effects. The author maintains that further research, based on reliable long-term experimental treatment studies, is sorely needed.
Forsinket søvnfasesyndrom er en av de mest utbredte søvnforstyrrelsene blant barn, ungdom og yngre voksne. Artikkelen drøfter diagnostikk, årsaksforhold og behandling.
En 24 år gammel kvinne kontakter sin primærlege og ber om sovemedisin til hjelp for store innsovningsvansker. Etter en tids arbeidsledighet har hun fått ny jobb som innebærer fleksibel arbeidsstart mellom kl 0700 og kl 0830. Hun frykter at hun ikke vil være opplagt eller klare å våkne tidsnok på grunn av sitt søvnproblem. Tidligere har hun blitt oppsagt fra to arbeidsforhold grunnet problemet. Pasienten har slitt med innsovningsvanskene siden tenårene. Når hun omsider sovner inn pleier hun å sove godt, og hun har vansker med å våkne om morgenen. Hun var ofte søvnig og ukonsentrert da hun gikk på skolen og ble tvunget opp av sengen kl 0700. Ofte klarte hun ikke å våkne om morgenen, men sov i stedet til langt utpå formiddagen og kom da mange timer for sent. Foreldrene kjempet en ofte håpløs kamp for å vekke henne. På grunn av denne atferden ble hun betraktet som lat og umotivert. I en utredning fra PPT under hennes skolegang, ble det konkludert med at skoleprestasjonene var langt lavere enn hennes evnenivå skulle tilsi. Mange ganger har hun prøvd å legge seg tidlig om kvelden, men klarer likevel ytterst sjelden å sove før kl 0200. Hun er fortvilet og nedstemt over problemet, og er redd hennes yrkeskarriere skal bli like skadelidende som hennes skolegang.
Denne kasusbeskrivelsen er trolig ikke ukjent for en del tenåringsforeldre, lærere, arbeidsgivere og helseprofesjonelle. Mange forklarer symptomene med lathet, manglende motivasjon og likegyldighet. Få innser at symptombildet er forenlig med døgnrytmeforstyrrelsen «forsinket søvnfasesyndrom», som er en av de mest utbredte søvnforstyrrelsene blant barn, ungdom og yngre voksne.
Denne artikkelen omhandler diagnostikk, forekomst, årsaksforhold og aktuelle behandlingstilnærminger ved dette søvnproblemet. Innledningsvis vil jeg gi en kort redegjørelse for sentrale søvnreguleringsmekanismer.
Søvnreguleringsmekanismer
For å forstå årsaksmodeller og behandlingsprinsipper for døgnrytmeforstyrrelser, trengs kunnskap om grunnleggende mekanismer for søvnregulering. Generelt kan en si at søvnen reguleres av tre samspillende faktorer (døgnrytme, homeostatiske mekanismer og atferd/vaner).
Hos mennesker og andre pattedyr er det døgnrytme eller cirkadian (gresk: cirka = omtrent, dias = dag) rytme i mange av kroppens funksjoner. Eksempler er utskillelse av hormoner som melatonin og kortisol, fordøyelse, kroppstemperatur og veksling mellom søvn og våkenhet Disse rytmene har en periode på om lag 24 timer. Temperaturrytmen har et minimum (nadir) tidlig om morgenen, normalt mellom kl 0400 og 0600. Fra nadir stiger kroppstemperaturen frem til et platå kl 1300–1500. Toppunktet i en slik rytme kalles for akrofase. Temperaturen holder seg på dette nivået frem til kl 2000–2200 om kvelden, før den begynner å synke ned mot nadir. Søvnen er normalt plassert fra ca. seks timer før til ca. to timer etter nadir for kroppstemperatur. Evnen til å sove er lav om morgenen, litt høyere mellom kl 1400 og kl 1700, og avtar igjen inntil den stiger en gang mellom kl 2100 og kl 0100 (Ursin, 1996). Denne stigningen er trolig knyttet til økning i melatoninutskillelse som finner sted i mørke om kvelden. Årsaken til den økende evnen til å sove mellom kl 1400 og kl 1700 er ikke kjent, og det finnes ikke noe tilsvarende fall i temperaturrytmen i dette tidsrommet.
Døgnrytmen (den cirkadiane rytmen) kontrolleres av nucleus suprachiasmaticus (SCN) i hypothalamus, som har en egenrytme (endogen) på omlag 25 timer. Dette innebærer at hos personer som totalt isoleres fra omverdenen vil døgnet bli ca. 25 timer langt. Normalt vil imidlertid den endogene rytmen justeres til en 24 timers rytme av ytre påvirkninger (såkalte «zeitgebers» eller tidsgivere), hvorav lys er den viktigste (Czeisler et al., 1989). Lys påvirker SCN via fiberforbindelser (tractus retinahypothalamicus) fra netthinnen. Kjernen projiserer til epifysen der melatonin produseres. Derfor viser også melatonin-produksjonen døgnrytme. Denne er nærmest et speilbilde av temperaturrytmen, med maksimum i 0400–0500 tiden om morgenen. Produksjonen av melatonin («mørkets hormon») hemmes av lyspåvirkning (Ursin, 1996). Det finnes melatoninreceptorer flere steder i sentralnervesystemet (særlig i SCN og i anterior hypofyse). Hormonet er trolig involvert i reguleringen av døgnrytmen i flere fysiologiske prosesser (von Gall Stehle, & Weaver, 2002).
Den andre søvnregulerende faktoren er den homeostatiske, og innebærer at et søvnbehov akkumuleres fra en våkner. Dette er nært knyttet til deltasøvn, da mengden deltasøvn (dyp søvn) som inntreffer under en søvnperiode er positivt forbundet med lengden av den forutgående våkenhetsperioden. Under søvnen svekkes det homeostatisk styrte søvnbehovet eksponentielt med tiden. Oppbyggingen av dette søvnbehovet i våken tilstand tar lengre tid enn svekkelsen som finner sted under søvn. Søvnigheten, det vil si tilbøyeligheten til å falle i søvn, vil derfor også være influert av den homeostatiske faktoren (Borbèly, 1982).
Vaner og atferd utgjør den tredje søvnregulerende faktoren. Atferd som innebærer at man reduserer stimulustilgangen fra ulike kilder, som fysisk aktivitet, støy, lys og koffein, og indre forhold som for eksempel bekymringer, vil fremme deaktivering og gjøre det lettere å sove.
En persons søvntilbøyelighet vil til enhver tid utgjøres av samspillet mellom den cirkadiane rytmen, homeostatiske mekanismer og atferd (Ursin 1996). Midt på natten vil for eksempel alle de tre faktorene normalt tilsi at man skal sove. (Dette er forutsatt at man har normal cirkadian rytme, at man ikke har sovet på dagtid og at man klarer å redusere stimulitilgangen.) Hos en nattarbeider tilsier både den homeostatiske og den cirkadiane faktoren at personen burde sove om natten, men han/hun klarer (som regel) likevel å holde seg våken, ved hjelp av bevegelse, samtale med andre, og inntak av stimulerende substanser som koffein. Atferdsfaktoren kan også forklare at noen kan sovne under en kjedelig forelesning i et mørkt rom kl 1000 om formiddagen, selv om både den homeostatiske og den cirkadiane faktoren tilsier at det skulle være lett å holde seg våken. Redusert stimulering til hjernen forklarer dermed den uimotståelige søvnigheten i slike sammenhenger (Bjorvatn & Holsten, 1997).
Døgnrytmeforstyrrelser – en oversikt
I henhold til ICD-10 er døgnrytmeforstyrrelse definert som fravær av synkronisering mellom personens søvn–våkenhetsrytme og den ønskede søvn–våkenhetsrytmen i forhold til miljøet, noe som resulterer i subjektive klager over søvnløshet eller hypersomni (World Health Organization, 1992, s. 186). Tilsvarende beskrivelser finnes i DSM-IV-TR (American Psychiatric Association, 2000) der fire kriterier spesifiseres (se Tabell 1). Man skiller normalt mellom flere undertyper av døgnrytmeforstyrrelser. Den mest detaljerte differensiering finnes i «International Classification of Sleep Disorders» (American Sleep Disorders Assocation, 1990) der seks undertyper beskrives:
Forsinket søvnfasesyndrom innebærer at hovedsøvnperioden er forsinket i forhold til det ønskede tidspunkt, noe som resulterer i innsovningsvansker eller vansker med å våkne til ønsket tid.
Fremskyndet søvnfasesyndrom er en forstyrrelse der hovedsøvnperioden er fremskyndet i forhold til det ønskede tidspunktet. Dette resulterer i sterk søvnighet tidlig på kvelden, tidlig innsovningstidspunkt og oppvåkning som inntrer tidligere enn ønsket.
Ikke-24-timers søvn–våkenhetssyndrom (frittløpende mønster) består av et kronisk stabilt mønster av forsinkelser i innsovningstids og oppvåkningstid med 1–2 timer per døgn.
Irregulært søvn–våkenhetsmønster representerer tidsmessige disorganiserte og variable episoder av søvn og våkenhet gjennom døgnet.
Tidssoneendringssyndrom (jet lag) består av vansker i varierende grad med å initierte eller å opprettholde søvn, uttalt søvnighet, nedgang i subjektiv våkenhet og prestasjoner, og somatiske symptomer (i stor grad knyttet til gastrointestinal funksjon) etter hurtig forflytning over flere tidssoner.
Skiftarbeidsforstyrrelse innebærer symptomer på insomni eller uttalt søvnighet som oppstår som et forbigående fenomen i forbindelse med arbeidstidsordningen.
Tabell 1. Diagnostiske kriterier for cirkadian søvnrytmeforstyrrelse i henhold til DSM-IV-TR (American Psychiatric Association, 2000, s. 629).
A. |
Vedvarende eller tilbakevendende mønster av søvnavbrudd som fører til overdreven søvnighet eller insomni, som er forårsaket av et misforhold mellom det søvn–våkenhetsmønster som kreves av personens omgivelser og hans eller hennes cirkadiane søvn–våkenhetsmønster. |
B. |
Søvnforstyrrelsen forårsaker klinisk betydningsfullt ubehag eller funksjonssvikt sosialt, arbeidsmessig eller på andre viktige områder |
C. |
Søvnforstyrrelsen forekommer ikke bare i forløpet av en annen søvnforstyrrelse eller en annen psykisk lidelse |
D. |
Forstyrrelsen skyldes ikke direkte fysiologiske virkninger av en substans (for eksempel en misbrukssubstans, et medikament eller en generell somatisk tilstand). |
Forsinket søvnfasesyndrom – diagnostiske vurderinger
De første som beskrev forsinket søvnfasesyndrom i forskningslitteraturen var Weitzman et al. (1981). Disse fant at blant 450 pasienter som søkte hjelp for innsovningsvansker hadde 30 dette søvnproblemet. Typisk var at disse pasientene ikke sovnet før mellom 0200 og 0600. De hadde ellers vansker med å våkne når de skulle for å komme tidsnok på skole eller jobb. Ofte var de søvnige på dagtid på grunn av lite nattesøvn. I helger og ferier når pasientene ikke måtte følge et bestemt tidsskjema var søvnlengden normal, og de våknet vanligvis spontant, men sent. De fleste av pasientene hadde prøvd mange metoder, som sovemedisin, alkohol, psykoterapi og kjerringråd, for å sovne inn tidligere, men uten suksess. Pasientene fortalte at de fungerte best, var mest opplagt og produktive sent på kvelden eller i de tidlige nattetimer.
I dag er dette en egen diagnose i «International Classification of Sleep Disorders» (se Tabell 2). Diagnosen stilles normalt ut fra minimumskriteriene A–E, men disse kan suppleres med målinger basert på polysomnografi og kontinuerlige temperaturmål (kriteriene F–G; American Sleep Disorders Assocation, 1990). Dette er imidlertid ikke realistisk i en klinisk sammenheng. Dessuten har man i det siste gått bort fra polysomnografi som diagnostisk instrument ved forsinket søvnfasesyndrom. I dag anbefales å stille diagnosen på grunnlag av et klinisk intervju og en uke med søvndagbok og/eller aktigrafi. Målinger basert på søvndagbok/aktigrafi bør gjøres uten at pasienten følger et bestemt tidsskjema, for eksempel i forhold til skole og jobb, ellers risikerer en å få maskerte data (Dagan, 2002a). En søvndagbok bør innholde spørsmål om: a) når man legger seg og står opp av sengen, b) innsovningstid, c) antall og varighet av oppvåkninger fra søvnen, d) tidspunkt for siste oppvåkning, e) subjektiv opplevd søvnkvalitet/dybde, f) søvnighet på dagtid, g) soving/blunding på dagtid og h) medikasjon/alkoholbruk i søvnøyemed (Lichstein & Riedel, 1994). Aktigrafi er målemetode der pasienten bærer en registreringsenhet på armen (som et ur). Denne lagrer informasjon om bevegelse og tidspunkt. På basis av en algoritme kan en ut fra denne informasjonen lage gode estimater av søvn og våkenhetsperioder til pasienten (Littner et al., 2003). Data fra søvndagbøker og/eller aktigrafi vil som regel vise at pasienter med forsinket søvnfasesyndrom sjelden sovner inn før 0200, ofte langt senere (American Sleep Disorders Association, 1990, s. 129).
Differensialdiagnoser
Klinikeren bør kjenne til sentrale differensialdiagnoser og komorbide tilstander. Forsinket søvnfasesyndrom har innsovningsvansker som kardinalsymptom, men bør skilles fra atferden man finner hos dem man populært omtaler som B-mennesker. B-mennesker foretrekker ofte å være sent oppe, og opplever at de fungerer best om kvelden. De kan ha vansker med å våkne om morgenen, og føler seg ofte søvnig på dagtid, særlig mot slutten av arbeidsuken. Ofte kan søvnfasen bli forsinket i helger slik at disse får problemer med å sovne inn søndag kveld eller de første dagene etter friperioder. Noen betrakter forskjellene mellom B-mennesker og pasienter som lider av forsinket søvnfasesyndrom som kvantitative (Pollak, 2000). Andre hevder imidlertid at forskjellene er kvalitative. I henhold til dette synet er pasienter med forsinket søvnfasesyndrom særlig karakterisert ved rigiditet i de cirkadiane rytmene, mens B-mennesker mer er kjennetegnet av fleksibilitet i disse (Dagan & Eisenstein, 1999). Uansett vil B-mennesker kunne oppleve innsovingsproblemer og tretthet på dagtid på grunn av sin atferdspreferanse. Differensialdiagnostiske betraktninger må derfor i slike tilfeller baseres på graden av problemet, evnen/fleksibilitet til å kunne endre rytme/søvnfase når dette er påkrevd og også delvis på behandlingsrespons. B-mennesker vil kunne endre sin søvnfase relativt lett ut fra søvnhygieniske prinsipper (se under behandling), mens pasienter med forsinket søvnfasesyndrom normalt vil profittere mindre på slike tiltak alene.
Tabell 2. Diagnostiske kriterier for forsinket søvnfasesyndrom i henhold til International Classification of Sleep Disorders (American Sleep Disorders Assocation, 1990, s. 132–133).
A. |
Manglende evne til å sovne inn eller å våkne opp på ønsket tidspunkt, eller uttalt søvnighet. |
B. |
Hovedsøvnperioden er forsinket i henhold til den ønskede tidsrammen for søvn. |
C. |
Symptomene har vært til stede minst 1 måned. |
D. |
Når personen ikke må følge et bestemt tidsskjema (for eksempel i ferier) vil pasientene:
|
E. |
Evidens for forsinkelse i pasientens vanemessige søvnperiode vises i søvndagbok ført daglig i minst to uker. |
F |
Laboratoriumbasert evidens for forsinkelse i tidspunkt for den vanemessige søvnen vist ved:
|
G |
Tilfredsstiller ikke kriteriene for en annen søvnlidelse som forårsaker vansker med å initiere søvn eller uttalt søvnighet. |
Kriteriene |
A–E er minimumskriterier for å stille diagnosen. |
I noen tilfeller er symptomene forenlig med forsinket søvnfasesyndrom motivert ut fra et ønske om å unngå skolegang og å holde seg borte fra jevnaldrende. Hos denne gruppen ser man at symptomene paradoksalt nok bedres i ferier. Betegnelsen motivert søvnfaseforsinkelse brukes derfor om dette fenomenet. Da symptomene er motivert ut fra sekundærgevinster, bør eventuell behandling rettes mot disse (Ferber & Boyle, 1983). En subgruppe pasienter som lider av primær insomni kan også ha store innsovningsvansker (for eksempel på grunn av bekymringer, lærte negative assosiasjoner til sengen og soverommet eller uheldige søvnvaner), men de våkner som regel spontant til adekvat tid om morgenen (Pallesen, 2002). En annen lidelse som er forbundet med innsovningsvansker er urolige bein («restless legs»). Symptomene her er stikkende, krypende og maurende sansefornemmelser fra bena, som kommer når en sitter eller ligger i ro, oftest om kvelden. Pasienten opplever da en sterk trang til å bevege bena, og ubehaget forsvinner som regel ved bevegelse (Montplaisir, Nicolas, Godbout & Walters, 2000). Bortsett fra innsovningsvanskene er disse symptomene ikke karakteristiske for forsinket søvnfasesyndrom.
Noen betrakter forskjellene mellom B-mennesker og pasienter som lider av forsinket søvfasesyndrom som kvantitative. Andre hevder at forskjellene er kvalitative
Et annet sentralt symptom ved forsinket søvnfasesyndrom er søvnighet på dagtid (særlig når man tvinges opp relativt tidlig om morgenen). Søvnighet er også et symptom ved narkolepsi. Søvnigheten er imidlertid sterkere hos narkoleptikere, som ofte kan sovne mens de utfører en oppgave. Narkoleptikere har i tillegg ofte andre symptomer som er distinkte, særlig katapleksi (som man finner hos ca. 70 % av narkoleptikerne). Katapleksi oppstår ofte ved opplevelse av emosjoner (som for eksempel overraskelse og frykt), og innebærer fall i muskeltonus, som kan resultere i alt fra svikt i knær og redusert kraft i en arm, til at pasienten bokstavelig ikke klarer å holde seg oppreist. Gjentatte episoder med søvnparalyse (forbigående lammelser av skjelettmusklatur) ved innsovning eller oppvåkning rammer 40–50 % av narkoleptikerne. Hypnagoge hallusinasjoner (som regel auditive eller visuelle hallusinasjoner ved innsovning/oppvåkning) og fragmentert/forstyrret nattesøvn, er også vanlig. Innsovningstiden er imidlertid kort. Kort innsovningstid finner man også hos pasienter med idiopatisk hypersomni. Likheten disse har med pasienter med forsinket søvnfasesyndrom er søvnighet på dagtid og vansker med å våkne om morgenen. Pasienter med idiopatisk hypersomni har behov for svært mye søvn, men selv når de oppnår dette, er de ofte søvnige på dagtid (Brooks & Mignot, 2002). Ved mistanke om narkolepsi/idiopatisk hypersomni bør pasientene henvises til polysomnografisk utredning (Pallesen, 2003). Pasienter med vinterdepresjon har også vansker med å våkne om morgenen, og søvnbehovet synes stort. Foruten generelle symptomer på depresjon, er disse pasientene karakterisert ved overspising, søthunger og vektøkning. Det foreligger data som indikerer at disse pasientene trolig har forsinket døgnrytme. Pasienter med vinterdepresjon har imidlertid i motsetning til pasienter med forsinket søvnfasesyndrom normalt ikke store innsovningsproblem. Symptomene ved vinterdepresjon følger dessuten et klart syklisk mønster, hvor symptomene typisk starter om høsten og hvor spontan remisjon inntrer på vårparten (Magnusson & Boivin, 2003).
I likhet med pasienter med forsinket søvnfasesyndrom, har pasienter med ikke-24 timers søvn–våkenhetssyndrom også en åpenbar døgnrytmeforstyrrelse. Pasienter med forsinket søvnfasesyndrom følger et stabilt, men forsinket 24-timers-mønster med hensyn søvn og våkenhet. Hos pasienter med ikke-24-timers søvn–våkenhetssyndrom finner det imidlertid sted en kontinuerlig forsinkelse av søvn–våkenhetsrytmen med 1–2 timer per døgn. Sistnevnte syndrom er meget sjeldent og forekommer oftest hos blinde (Zammit, 1997).
Komorbiditet
Studier har vist at forsinket søvnfasesyndrom har høy komorbiditet med andre tilstandsbilder. I en studie ble det for eksempel funnet at ca. 20 % av unge pasienter med forsinket søvnfasesyndrom hadde læringsvansker. Dette ble forklart med at søvnvanskene hemmet oppmerksomhet og læring på skolen (Dagan & Eisenstein, 1999). Personlighetsforstyrrelser, særlig karakterisert ved affektlabilitet, er også funnet å være overhyppig hos pasienter med forsinket søvnfasesyndrom. Det antas at døgnrytmeforstyrrelser og personlighetsforstyrrelser gjensidig innvirker på hverandre (Dagan, Stein, Steinboch, Yovel & Hallis, 1998).
Forsinket søvnfasesyndrom er også knyttet til depresjon. Normalt er depresjon forbundet med tidlig morgenoppvåkning. Mange depressive føler seg imidlertid best om kvelden, og utsetter derfor ofte søvnen. Dette kan hos noen lede til forsinkelse av søvnfasen. Forsinkelse av søvnfasen kan i seg selv også føre til eller forsterke depresjon, mens fremskyndelse av søvnfasen kan virke antidepressivt (Regestein & Monk, 1995; Regestein & Pavlova, 1995). Det er en stor mengde evidens som antyder tilstedeværelse av underliggende døgnrytmeforstyrrelse ved affektive lidelser (Van den Hoofdakker, 1994). Samlet sett virker det rimelig å anta en gjensidig årsakssammenheng mellom affektive forstyrrelser og døgnrytmeforstyrrelser (Lustberg & Reynolds, 2000).
Forekomst
Forsinket søvnfasesyndrom antas å være den mest utbredte av døgnrytme-forstyrrelsene (Dagan & Eisenstein, 1999). I epidemiologiske studier basert på større befolkningsutsnitt har man imidlertid funnet relativt lav forekomst. I en norsk studie basert på et utvalg på 10 000 tilfeldige personer, 18–67 år gamle (responsrate 77 %), ble det bare funnet en prevalens på 0.17 %. Det var ingen sammenheng med alder og prevalens. I studien undersøkte man også utbredelsen av ekstrem kveldspreferanse (ekstreme B-mennesker). Dette var definert som oppfyllelse av kriteriene A–E for forsinket søvnfasesyndrom (se Tabell 1), men der respondentene var i stand til å fremskynde innsovningstidspunktet til før 0100 når jobb eller skoleforpliktelser tilsa dette. Utbredelsen av ekstrem kveldspreferanse var 0.72 %. Her fant man en klar sammenheng med alder. Utbredelsen av ekstrem kveldspreferanse var 4.6 % blant 18–19-åringer, mens den var langt lavere blant de andre aldersgruppene. Blant de eldste i utvalget, 60–67 år, forekom ikke ekstrem kveldspreferanse hos noen av respondentene (Schrader, Bovim & Sand, 1993). I en tilsvarende japansk befolkningsstudie fant man også lav prevalens, 0.13 %, av forsinket søvnfasesyndrom (Yazaki, Shirakawa, Okawa, & Takahashi, 1999). I en amerikansk studie basert på et tilfeldig utvalg av 417 personer mellom 40 og 60 år ble prevalensen av forsinket søvnfasesyndrom estimert til 0.7 % (Ando, Kripke & Ancoli-Israel, 1995). Relativt høy prevalens av forsinket søvnfasesyndrom har man imidlertid funnet i studier av ungdom. I en studie blant respondenter mellom 12 og 20 år fant man en prevalensrate på 1.3 % (LeBlanc et al., 1999), mens man i en annen studie på ungdom (12–19 år) fant en forekomst på 7.3 %. Denne undersøkelsen var imidlertid bare basert på 109 respondenter (Pelayo, Thorpy & Glovinsky, 1988). Det er konsensus på feltet om at en vet lite om utbredelsen av forsinket søvnfasesyndrom (Dagan, 2002b), og at flere epidemiologiske studier er påkrevd. En utbredt oppfatning er at syndromet vanligvis debuterer i tenårene eller i tidlig voksen alder, men en stor del av pasienter rapporterer at symptomene startet i tidlig barndom. Det ser ikke ut til å være kjønnsforskjeller i utbredelsen (Dagan & Eisenstein, 1999).
Årsaksforhold
Sosiale faktorer, vaner og biologiske faktorer er trolig sentrale årsakskomponenter. Uheldige søvnvaner bidrar trolig en del. Å være lenge oppe i helger og ferier, og å sove langt utpå dagen i disse fasene, kan vanskeliggjøre innsovning når en senere ønsker at døgnrytmen skal fremskyndes. En livsstil uten daglige tidsrammer å forholde seg til er også en miljøfaktor som kan bidra til at syndromet utvikles. Forsinket søvnfasesyndrom har derfor populært blitt omtalt som «frilanser-syndromet». Ungdom og andre som er lenge oppe om kveldene og nettene blir ofte søvnig på dagtid. En del av disse faller derfor for fristelsen til å sove på ettermiddagen. Denne atferden vanskeliggjør innsovning til ønsket tid om kvelden, grunnet svekkelse av den homeostatiske søvnfaktoren. Dermed kan en komme inn i en ond sirkel som fremmer utvikling av syndromet (Whyte & Schaefer, 1995).
Mulighetene for rekreasjon og aktivitet om natten har økt dramatisk. For mange bidrar dette til at innsovningstidspunktet forsinkes
Samfunnet har i løpet av de siste tiår gått i retning av et såkalt «24-timers samfunn» hvor ulike servicetilbud i stadig større grad er døgnåpne. Gjennom tekniske nyvinninger som TV, datamaskiner, internett og mobiltelefoner, har muligheter for rekreasjon og aktivitet om natten økt dramatisk (Ferrara & De Gennaro, 2001). For mange bidrar dette til at innsovningstidspunktet forsinkes.
Inntak av koffein og nikotin virker stimulerende på sentralnervessystemet, og kan bidra til innsovningsvansker og trolig også lede til forsinket søvnfase (Stores, 2001). Nattarbeid kan muligens også være en utløsende miljøfaktor (Czeisler et al., 1981).
Under puberteten ser det ut til å inntreffe en biologisk basert forsinkelse på om lag to timer av den cirkadiane rytmen (Carskadon, Vieira & Acebo, 1993), parallelt med at søvnbehovet ser ut til å økes noe (Carskadon et al., 1980). Studier tyder imidlertid på at ungdom ikke forholder seg til dette. I en studie på norske 17-åringer ble det for eksempel funnet at de i gjennomsnitt sov 7,3 timer på hverdager og 10,1 timer i helgene. På hverdagene la de seg i gjennomsnitt senere (kl 2330) enn det som normalt er anbefalt, og enda senere i helgene (kl 0130). Det konkluderes fra undersøkelsen med at ungdommene som gruppe så ut til å ha forsinket søvnfase (Sørensen & Ursin, 2001).
Studier har ellers vist at visse medikamenter, som for eksempel haloperidol og fluvoksamin, muligens kan forårsake forsinket søvnfasesyndrom. Hodetraumer kan også gi slike symptomer. I de sistnevnte tilfeller vil tradisjonell behandling av forsinket søvnfasesyndrom trolig ikke gi særlig effekt, men behandlingen bør i stedet rette seg mot rehabilitering av hodeskaden (Dagan, 2002a).
Til tross for at det er mange vaner og miljøfaktorer som bidrar til å forsinke søvnfasen, vil de fleste være i stand til å fremskynde den når det er påkrevd. For et mindretall fremstår imidlertid dette som svært vanskelig. Flere studier tyder på at i tillegg til atferd og miljøfaktorer bidrar biologiske faktorer også til utvikling og opprettholdelse av symptomene. De fleste av disse er knyttet til anomalier ved de cirkadiane reguleringsmekanismene. Normalt vil lyseksponering før nadir forsinke den cirkadiane rytmen, mens denne blir fremskyndet ved lyseksponering etter nadir. Studier har vist at tiden fra nadir til spontan oppvåkning er lengre hos pasienter med forsinket søvnfasesyndrom sammenliknet med tiden til friske kontrollpersoner (Ozaki, Uchiyama, Shirakawa & Okawa, 1996). Dette innebærer at pasienter med forsinket søvnfasesyndrom i større grad enn andre er tilbøyelig til å sove på tidspunkter der de er særlig sensitive for fasefremskyndende effekter av lys. Mange forskere har antydet at personer med særlig lang endogen cirkadiane periode (opptil 25,5 timer) kan ha vansker med å justere denne til en periode på 24 timer, særlig dersom lysstimuleringen ikke er optimal (Regestein & Monk, 1995). Det har også blitt framsatt hypoteser om at det biologiske potensialet for fasefremskyndelse er mindre hos disse pasientene enn hos friske personer (Czeisler et al., 1981). Andre har antatt at pasientene har nedsatt sensitivitet for lys, og at dette medfører at den endogene rytmen i redusert grad blir justert til en 24 timers periode. I en studie ble det imidlertid funnet at slike pasienter fikk sterkere undertrykning av melatoninproduksjonen enn friske personer ved lyseksponering. Det kan tyde på at pasienter med forsinket søvnfasesyndrom er hypersensitive for lys. Symptomene forstås dermed som en konsekvens av lyseksponering på tidspunkter (om kvelden) som gir faseforsinkelse (Aoki, Ozeki & Yamada, 2001).
I en studie fant Uchiyama et al. (2000) at pasienter med forsinket søvnfasesyndrom i langt mindre grad enn friske personer kunne sovne inn tidligere enn vanlig etter en periode med søvndeprivasjon. Det så altså ut som at den homeostatiske søvnfaktoren i liten grad kunne fremskynde søvnfasen hos disse pasientene. Det ble også funnet at tiden fra melatoninproduksjonen nådde et visst nivå om kvelden og til søvnighet inntrådte, var lengre hos pasientene enn hos friske personer.
En annen og mindre omtalt hypotese ble lansert av Daan og Pittendrigh (1976). De hevdet at jo kortere den endogene periode var, desto mer sannsynlig ville det være at en tilfeldig lyspuls ville ha faseforsinkende effekt. En skulle således tro at pasienter med forsinket søvnfasesyndrom hadde særlig kort endogen cirkadian periode. Generelt er det således en god del evidens som peker i retning av svikt i de cirkadiane reguleringsmekanismene som en viktig årsak ved forsinket søvnfasesyndrom. En har videre antatt at disse er knyttet til genetiske faktorer. I en del nyere studier har en også funnet genetiske markører som klart ser ut til å være forbundet med forsinket søvnfasesyndrom (Archer et al., 2003; Hohjoh et al., 2003).
Oppsummert er det grunn til å betrakte syndromet som en forstyrrelse med rot i biologi, atferd og bestemte miljøpåvirkninger.
Behandling
Behandling består av lysterapi, vitamin B12, melatonin, kronoterapi og søvnhygiene.
Lysterapi
Ved lysterapi eksponeres pasienten for lys i den synlige delen av spectrum (380–760 nm). Normalt brukes lys med høy intensitet (2500–10 000 lux). Jo høyere intensiteten er, desto lavere eksponeringstid er nødvendig. Ved 10 000 lux er vanlig eksponeringstid ca. 30 minutter (Terman & Terman, 2000). Ved døgnrytmeforstyrrelser er det helt avgjørende at lyset administeres på riktig tidspunkt, da effekten av lys følger en såkalt fase–respons-kurve (Khalsa, Jewett, Cajochen & Czeisler, 2003). Den sorte linjen i Figur 1 viser en fase–respons-kurve for en person med normal døgnrytme. For personer med forsinket søvnfasesyndrom vil fase–respons-kurven være forsinket i forhold til tidspunktene som vises i figuren. Normalt vil lys administrert før bunnpunktet i kroppstemperaturrytmen (nadir) gi faseforsinkelse, mens lys administrert etter nadir gir fasefremskyndelse (Bjorvatn & Holsten, 1997). Skal man oppnå fasefremskyndelse, vil man oppnå sterkest effekt ved å administrere lys i de første 3–4 timene etter nadir. I klinisk praksis kan en estimere nadir til to timer før spontan morgenoppvåkning. Spontant morgenoppvåkningstidspunkt er det tidspunkt pasienten våkner av seg selv når pasienten får sove så lenge han eller hun føler for. Dersom en pasient med forsinket søvnfasesyndrom våkner spontant kl 1200, kan nadir estimeres til ca. 1000. Når en starter lysterapi er det viktig å være sikker på at en eksponeringen ikke finner sted før nadir. For eksempel kan en i dette tilfelle vekke pasienten og starte lyseksponeringen kl 1100. En vanlig antakelse er at en kan fremskynde døgnrytmen med ca. en time per døgn. Neste behandlingsdag kan lyseksponeringen således finne sted kl 1000, en kan med andre ord fremskynde eksponeringstidpunktet med 1 time per døgn. Min egen erfaring er imidlertid at en del pasienter ikke klarer å fremskynde døgnrytmen med så mye som en time per døgn. For denne pasientgruppen vil fremskyndelse av eksponeringstidspunktet og døgnrytmen med 20–30 minutter per døgn trolig være mer realistisk.
Behandling består av lys-terapi, vitamin B12, melatonin, kronoterapi og søvnhygiene
En skal være oppmerksom på at dersom en vekker opp en pasient (for eksempel med nadir for kroppstemperatur kl 1000) tidlig om morgenen, vil dette medføre at all kunstig og naturlig lyseksponering frem til 1000 har en faseforsinkende og således symptom-eskalerende effekt. Lyseksponering før nadir bør derfor unngås for denne pasientgruppen, for eksempel ved å bruke solbriller. Når pasienten har kommet i riktig fase, kan en stoppe lyseksponeringen. For noen må imidlertid behandlingen pågå nærmest kontinuerlig for å hindre tilbakefall. Vedlikeholdsbehandling med lysterapi 2–4 ganger i uken kan også være aktuelt (Pallesen, Skjerve & Bjorvatn, i trykk).
I velkontrollerte eksperimentelle studier har en funnet at lyseksponering om morgenen har fasefremskyndet cirkadiane rytmer og gitt økt subjektiv våkenhet om morgenen (Cole, Smith, Alcalà, Elliott & Kripke, 2002; Rosenthal et al., 1990). Slike studier foreligger imidlertid i et meget lite antall, og en mangler studier med lang oppfølgingstid.
De vanligste bivirkningene ved lysterapi er hodepine, irriterte øyne og agitasjon. Som regel er disse av kortvarig natur. Det er ikke påvist at øyeskader har oppstått som følge av lysterapi innenfor de behandlingsregimer som anbefales. For pasienter med bipolare lidelser kan lysterapi muligens utløse maniske tilstander (Pallesen et al., i trykk).
Vitamin B12
Tidlige rapporter indikerte at vitamin B12 kunne ha god terapeutisk effekt (Okawa et al., 1990). I en nylig velkontrollert dobbelblind studie fant en imidlertid ingen virkning av vitamin B12 på subjektiv søvnighet eller søvn målt ved søvndagbok (Okawa et al., 1997). Imidlertid ser vitamin B12 ut til å forsterke effekten av lysterapi, trolig ved å gjøre de cirkadiane reguleringsmekanismene mer sensitive for lys (Hashimoto et al., 1996). Vitamin B12 kan dermed være nyttig som et supplement til lysterapi.
Melatonin
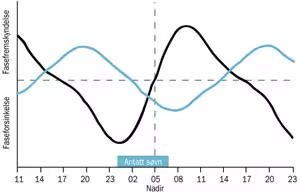
Figur 1. Fase–respons-kurve for lys (sort) og melatonin (blått) basert på studier av Khalsa et al. (2003) og Lewy et al. (1998). Forskjellen i styrken på effekten av lysterapi og melatonin vil ikke nødvendigvis være slik som det her er fremstilt, men vil være avhengig av lysintensitet, eksponeringstid og styrken på dosen av melatonin.
Eksogent melationin kan også fremkalle fasefremskyndelse. I likhet med effektene av lyseksponering følger effektene av melatonin også en fase–respons-kurve. I Figur 1 er en fase–respons-kurve for melatonin vist (blå linje) for en person med normal døgnrytme (nadir for kroppstemperatur kl 0500). Som det fremgår av denne kurven, vil melatonin ha en fasefremskyndende effekt når det administreres om kvelden, og en faseforsinkende effekt om morgenen (Lewy et al., 1998). En bør imidlertid være oppmerksom på at for pasienter med forsinket søvnfasesyndrom vil fase–respons-kurven også for melatonin være forsinket, det vil si forskjøvet mot høyre i forhold til det som vises på Figur 1. I klinisk praksis antas at en kan administrere melatonin 5–7 timer før pasientens ordinære innsovningstidspunkt for å oppnå fasefremskyndelse (Mundey et al., 2003).
Melatonin administreres vanligvis i doser mellom 0.3 og 5 mg og har trolig en viss sedativ effekt som oppstår via senket kroppstemperatur, i tillegg til en direkte effekt på døgnrytmen. Den fasefremskyndende effekten er noe bedre dokumentert enn den faseforsinkende (Arendt, 2000).
I en velkontrollert dobbel-blind be-handlingsstudie ble det funnet at melatonin gav kortere innsovningstid. På noen subjektive mål på tretthet og våkenhet viste resultatene bedring i melatoningruppen sammenliknet med placebogruppen. Biologiske indikatorer på døgnrytme indikerte at denne ble fasefremskyndet i melatoningruppen (Kayumov, Brown, Jindal, Buttoo, & Shapiro, 2001). I en annen studie med tilsvarende design ble det også funnet positive effekter av melatonin på flere søvn- og cirkadiane parametre, samt på våkenhet om morgenen (Nagtegaal, Kerkhof, Smits, Swart & Van der Meer, 1998). En trenger imidlertid flere velkontrollerte studier for å vurdere effekten av melatonin ved forsinket søvnfasesyndrom. Især mangler langtidsstudier.
I Norge er melatonin tilgjengelig, men legen må søke om det på registreringsfritak. Ved de doser som vanligvis benyttes tolereres melatonin som regel meget godt, og det er ikke rapportert om alvorlige bivirkninger. I en studie ble det imidlertid funnet at melatonin var forbundet med langvarig svekkelse av sædkvalitet hos menn (Luboshiyzky, Shen-Orr, Nave, Lavi & Lavie, 2002). Melatonin passerer placenta og over i morsmelk. En vet lite om teratogenitet, interaksjonseffekter, langtidseffekter og effekter på det reproduktive system. Det er uenighet om melatonin på generell basis kan anbefales som terapi (Arendt, 1997). Ofte benyttes både melatonin- og lysterapi samtidig (Baker & Zee, 2000). Det er da vanlig å administrere melatonin ca. 12 timer før lysterapien.
Kronoterapi
Kronoterapi er en atferdsbasert form for terapi. Den ble opprinelig beskrevet av Czeisler et al. (1981), og tok utgangspunkt i at pasientene manglet egen evne til å fasefremskynde søvn–våkenhetsrytmen. Kronoterapi består av to faser. I fase 1 faseforsinkes søvn–våkenhetsrytmen med 3 timer per døgn inntil pasienten når de ønskede innsovnings- og oppvåkningstidspunkter (se Figur 2). Denne fasen varer normalt 5–7 døgn. Målet i fase 2 er å opprettholde endringene, og innebærer at pasienten da må unngå å faseforsinke søvn–våkenhetsrytmen. Pasienten må derfor ikke stå opp senere enn vanlig på fridager, i helger og ferier (Czeisler et al., 1981).

Figur 2. Oversikt over mulig faseforsinkelse ved kronoterapi ved forsinket søvnfasesyndrom.
Sheldon, Spire og Levy (1992) mener i motsetning til Czeisler et al. (1981) at man også kan fasefremskynde søvn–våkenhetsrytmen ved hjelp av kronoterapi. Slik fasefremskyndelse er særlig aktuell der faseforsinkelsen i utgangspunktet er tre timer eller mindre. I denne formen for kronoterapi fremskyndes leggetidspunktet og oppvåkningstidspunktet med ca. 15 minutter hver dag inntil ønsket fase nås. I noen tilfeller kombineres dette med søvnrestriksjon. Det innebærer at pasienten i starten forskyver oppvåkningstidspunktet relativt mer enn innsovningstidspunktet. En pasient som normalt sovner kl 0400 og våkner kl 1100, kan for eksempel de neste fem dagene legge seg henholdsvis kl 0345, 0330, 0315, 0300 og 0245, mens de korresponderende oppvåkningstidspunktene kan være kl 1030, 1000, 0930, 0900 og så 0845 osv. Alternativt kan en vekke personen opp ved ønsket tidspunkt, for eksempel kl 0700, fra første dag i behandlingen, og så gradvis fremskynde leggetidspunktet (Mindell & Owens, 2003). Ved hjelp av de sistnevnte metoder forsøker en å utnytte den homeostatiske søvnreguleringsfaktoren for å fremme fasefremskyndelse.
Kronoterapi er forholdsvis sjeldent benyttet. Det er lite forskningsmateriale tilgjengelig som dokumenterer metodens effektivitet (Dagan, 2002b).
Søvnhygiene
Søvnhygiene innebærer konkrete råd om hvordan man skal opptre for å unngå søvnproblemer. Med hensyn til forsinket søvnfasesyndrom vil slike råd ha særlig relevans med tanke på å opprettholde terapeutisk bedring, og å hindre eventuell ytterligere forverring av problemet. En god anbefaling er at man bør stå opp til et fast tidspunkt uansett hvor mye man har sovet. En bør videre unngå stimulering på kveldtid før leggetid. Slik uheldig stimulering initieres som regel gjennom mental aktivitet, som intellektuelt arbeid, bekymringer og krangling, fysisk aktivitet som kroppsarbeid og trening, eller via psykoaktive substanser som koffein og nikotin. En bør også avstå fra høneblunder og å sove middag (Stepanski & Wyatt, 2003).
Anbefalingene har i liten grad vært gjenstand for empiriske etterprøving i forhold til forsinket søvnfasesyndrom. Ut fra det en kjenner til om søvnreguleringsmekanismer er det likevel grunn til å anta at de vil kunne opprettholde behandlingsresultater oppnådd med andre terapiformer.
Praktiske sider ved behandling
Lysterapi er ofte tidkrevende for pasienten, og dette kan gi redusert føyelighet til behandlingsregimet (Pallesen et al., i trykk). Kronoterapi kan være forbundet med nedsatt vilje til å etterleve de terapeutiske retningslinjene. Melatoninbehandling blir ofte bedre akseptert av pasientene, men her vet man som nevnt lite om langstidseffekter. En skal også være oppmerksom på at lysterapi trolig har en noe bedre effekt enn melatonin ved de kliniske betingelser lys og melatonin vanligvis blir administrert under (Avery, Lenz & Landis, 1998). Tilbakefall er forholdsvis vanlig. En kan hindre dette ved å være nøye med søvnhygienen etter at ønsket søvn–våkenhetsrytme er nådd gjennom aktiv behandling som lysterapi eller melatoninadministrasjon. I mange tilfeller kan også vedlikeholdsbehandling, for eksempel 2–4 dager i uken med melatonin og/ eller lysbehandling, være aktuelt. Komorbide tilstander som depresjon bør eventuelt også kartlegges og behandles for at søvn-våkenhetsrytmen lettere skal bli korrigert (Burns, Sateia & Lee-Chiong, 2002). For personer som ikke oppfyller de diagnostiske kriteriene for forsinket søvnfasesyndrom, men som i mildere grad har forsinket døgnrytme (B-mennesker), kan naturlig lyseksponering i 30 minutter utendørs om morgenen, og etterlevelse av søvnhygienereglene, trolig lette innsovningen om kvelden (Dagan, Tzischinsky & Lavie, 1981; Harada, Morisane & Takeuchi, 2002; Zarcone, 1994). I en studie ble det også funnet at administrasjon av 6 mg melatonin på søndag ettermiddag kunne motvirke forsinkelse av søvnfasen som forsøkspersonene hadde pådratt seg i løpet av en helg (Yang et al., 2001). Regulær behandling av denne type drift av søvnfasen med melatonin kan imidlertid ikke anbefales ut fra nåværende kunnskapsnivå (Arendt, 1997).
Avslutning
Symptomene blir ofte oversett, attribuert til lathet, eller feilbehandlet
Det er liten kunnskap om forsinket søvnfasesyndrom blant helseprofesjonelle og blant personer som ellers på ulike måter steller med ungdom. Dette medfører at symptomene ofte blir oversett, attribuert til lathet, eller feilbehandlet. Dette er særlig uheldig, da forsinket søvnfasesyndrom ofte medfører dårlig fungering på flere sentrale arenaer som skole, jobb og i det sosiale liv. Det trengs derfor langt mer opplysning om lidelsen og dens symptomer. En trenger også flere epidemiologiske undersøkelser på feltet for å kunne vurdere den reelle utbredelsen av lidelsen. Det er behov for flere godt kontrollerte eksperimentelle behandlingsstudier, slik at en kan nå et kunnskapsnivå som gir klare anbefalinger for forebygging og behandling
Det er grunn til å tro at samfunnsutviklingen i retning av et «24-timers samfunn» bidrar til å øke forekomsten av dette søvnproblemet. Samtidig skal en også være oppmerksom på at «24-timers samfunnet» kan gi pasienter med forsinket søvnfasesyndrom økte muligheter til å delta i arbeidslivet og sosiale aktiviteter, uten å forandre sine circadiane tilbøyeligheter.
Referanser
American Psychiatric Association (APA). (2000). Diagnostic and statistical manual of mental disorders (4th ed., textrev.). Washington, DC: Author.
American Sleep Disorders Association. (1990). The international classification of sleep disorders. Diagnostic and coding manual. Rochester: Author.
Ando, K., Kripke, D. F., & Ancoli-Israel, S. (1995). Estimated prevalence of delayed and advanced sleep phase syndromes. Sleep Research, 24, 509.
Arendt, J (1997). Safety of melatonin in long-term use. Journal of Biological Rhythms, 12, 673–681.
Arendt, J. (2000). In what circumstances is melatonin a useful sleep therapy? Consensus statement, WFSRS Focus Group, Dresden, November 1999. Journal of Sleep Medicine, 9, 397–398.
Archer, S. N., Robilliard, D. L., Skene, D. J., Smits. M., Williams, A., Arendt, J., & von Schantz, M. (2003). A length polymorphism in the circadian clock gene Per3 is linked to delayed sleep phase syndrome and extreme diurnal preferences. Sleep, 26, 413–415.
Aoki, H., Ozeki, Y., & Yamada, N. (2001). Hypersensitivity of melatonin suppression in response to light in patients with delayed sleep phase syndrome. Chronobiology International, 18, 263–271.
Avery, D., Lenz, M., & Landis, C. (1998). Guidelines for prescribing melatonin. Annals of Medicine, 30, 122–130.
Baker, S. K., & Zee, P. C. (2000). Circadian disorders of the sleep-wake cycle. I M. H. Kryger, T. Roth, & W. C. Dement (Eds.), Principles and practice of sleep medicine (3rd ed., ss. 606–614). Philadelphia: W. B. Saunders Company.
Bjorvatn, B., & Holsten, F. (1997). Lysbehandling ved jet lag, nattarbeid og søvnlidelser. Tidsskrift for Den norske lægeforening, 117, 2489–2492.
Borbèly, A. A. (1982). A two-process model of sleep regulation. Human Neurobiology, 1, 195–204.
Brooks, S. N., & Mignot, E. (2002). Narcolepsy and idiopathic hypersomnia. I T. L. Lee-Chiong, M. J. Sateia, & M. A. Carskadon (Eds.), Sleep medicine (ss. 193–202). Philadelphia: Hanley & Belfus.
Burns, E. R., Sateia, M. J., & Lee-Chiong, T. L. (2002). Basic principles of chronobiology and disorders of circadian sleep-wake rhythm. I T. L. Lee-Chiong, M. J. Sateia & M. A. Carskadon (Eds.), Sleep medicine (ss. 245–254). Philadelphia: Hanley & Belfus.
Carskadon, M. A., Harvey, K., Duke, P., Anders, T. F., Litt, I. F., & Dement, W. C. (1980). Pubertal changes in daytime sleepiness. Sleep, 2, 453–460.
Carskadon, M. A., Vieira, C., & Acebo, C. (1993). Association between puberty and delayed phase preference. Sleep, 16, 258–262.
Cole, R. J., Smith, J. S., Alcalá, Y. C., Elliott, J. A., & Kripke, D. F. (2002). Bright-light mask treatment of delayed sleep phase syndrome. Journal of Biological Rhythms, 17, 89–101.
Czeisler, C. A., Kronauer, R. E., Allan, J. S., Duffy, J. F., Jewett, M. E., Brown, E. N., & Ronda, J. M. (1989). Bright light induction of strong (Type 0) resetting of the human circadian pacemaker. Science, 244, 1328–1333.
Czeisler, C. A., Richardson, G. S., Coleman, R. M., Zimmerman, J. C., Moore-Ede, M. C., Dement, W. C., & Weitzman, E. D. (1981). Chronotherapy: Resetting the circadian clocks of patients with delayed sleep phase insomnia. Sleep, 4, 1–21.
Daan, S., & Pittendrigh, C. S. (1976). Functional-analysis of circadian pacemakers in nocturnal rodents. 2. Variability of phase response curves. Journal of Comparative Physiology, 106, 253–266.
Dagan, Y. (2002a). Circadian rhythm sleep disorders (CRSD). Sleep Medicine Reviews, 6, 45–55.
Dagan, Y. (2002b). Circadian rhythm sleep disorders (CRDS) in psychiatry – A review. Israel Journal of Psychiatry and Related Sciences, 39, 19–27.
Dagan, Y., & Eisenstein, M. (1999). Circadian rhythm sleep disorders: Towards a more precise definition and diagnosis. Chronobiology International, 16, 213–222.
Dagan, Y., Stein, D., Steinboch, M., Yovel, I., & Hallis, D. (1998). Frequency of delayed sleep phase syndrome among hospitalized adolescent psychiatric patients. Journal of Psychosomatic Research, 45, 15–20.
Dagan, Y., Tzischinsky, O., & Lavie, P. (1981). Sunlight treatment for delayed sleep phase syndrome: Case report. Sleep Research, 20, 451.
Ferber, R., & Boyle, P. (1983). Delayed sleep phase syndrome versus motivated sleep phase delay in adolescents. Sleep Research, 12, 239.
Ferrara, M., & De Gennaro, L. (2001). How much sleep do we need? Sleep Medicine Reviews, 5, 155–179.
Harada, T., Morisane, H., & Takeuchi, H. (2002). Effects of daytime light conditions on sleep habits and morningness-eveningness preferences of Japanese students aged 12–15 years. Psychiatry and Clinical Neurosciences, 56, 225–226.
Hashimoto, S., Kohsaka, M., Morita, N., Fukuda, N., Honma, S., & Homna, K. (1996). Vitamin B12 enhances the phase-response of circadian melatonin rhythm to a single bright light exposure in humans. Neuroscience Letters, 220, 129–132.
Hohjoh, H., Takasu, M., Shishikura, K., Takahasi, Y., Honda, Y., & Tokunaga, K. (2003). Significant association of the arylalkylamine N-acetyltransferase (AA-NAT) gene with delayed sleep phase syndrome. Neurogenetics, 4, 151–153.
Kayumov, L., Brown, G., Jindal, R., Buttoo, K., & Shapiro, C. M. (2001). A randomized, double-blind, placebo-controlled crossover study of the effect of exogenous melatonin on delayed sleep phase syndrome. Psychosomatic Medicine, 63, 40–48.
Khalsa, S. B. S., Jewett, M. E., Cajochen, C., & Czeisler, C. A. (2003). A phase response curve to single bright light pulses in human subjects. Journal of Physiology, 549, 945–952.
LeBlanc, J. C., Morehouse, R., Rajda, M., Hayden, D., Thompson, S., & Rusuk, B. (1999). Prevalence of delayed sleep phase syndrome in adolescents: A school-based survey. Pediatric Research, 45, 5A.
Lewy, A. J., Bauer, V. K., Ahmed, S., Thomas, K. H., Cutler, N. L., Singer, C. M., Moffit, M. T., & Sack, R. L. (1998). The human phase response curve (PRC) to melatonin is about 12 hours out of phase with the PRC to light. Chronobiology International, 15, 71–83.
Lichstein, K. L., & Riedel, B. W. (1994). Behavioral assessment and treatment of insomnia: A review with an emphasis on clinical application. Behavior Therapy, 25, 659–688.
Littner, M., Kushida, C. A., Anderson, M., Bailey, D., Berry, R. B., Davila, D. G., Hishko-witz, M., Kapen, S., Kramer, M., Loube, D., Wise, M., & Johnson, S. F. (2003). Practice parameters for the role of actigraphy in the study of sleep and circadian rhythms: An update from 2002. An American academy of sleep medicine report. Sleep, 26, 337–341.
Luboshitzky, R., Shen-Orr, Z., Nave, R., Lavi, S., & Lavie, P. (2002). Melatonin administration alters semen quality in healthy men. Journal of Andrology, 23, 572–578.
Lustberg, L., & Reynolds, C. F. (2000). Depression and insomnia: Questions of cause and effect. Sleep Medicine Reviews, 4, 253–262.
Magnusson, A., & Boivin, D. (2003). Seasonal affective disorder: An overview. Chronobiology International, 20, 189–207.
Mindell, J. A., & Owens, J. A. (2003). A clinical guide to pediatric sleep. Diagnosis and management of sleep problems. Philadelphia: Lippicott Williams& Wilkins.
Monplaisir, J., Nicolas, A., Godbout, R., Walters, A. (2000). Restless legs syndrome and periodic limb movement disorder. I M. H. Kryger, T. Roth, & W. C. Dement (Eds.), Principles and practice of sleep medicine (3rd ed., ss. 742–752). Philadelphia: W. B. Saunders Company.
Mundey, K., Gourineni, R., Benloucif, S., Sethi, P., Wolfe, L. F., Guico, M. J., Ortiz, R., & Zee, P. C. (2003). Treatment of delayed sleep phase syndrome with melatonin: A practical approach. Sleep, 26, A312.
Nagtegaal, J. E., Kerkhof, G. A., Smits., M. G., Swart, A. C. W., & Van der Meer, Y. G. (1998). Delayed sleep phase syndrome: A placebo-controlled cross-over study on the effects of melatonin administered five hours before individual dim melatonin onset. Journal of Sleep Research, 7, 135–143.
Okawa, M., Mishima, K., Nanami, T., Shimizu, T., Iijima, S., Hishikawa, Y., & Takahashi, K. (1990). Vitamin B12 treatment for sleep-wake rhythm disorders. Sleep, 13, 15–23.
Okawa, M., Takahashi, K., Egashira, K., et al. (1997). Vitamin B12 treatment for delayed sleep phase syndrome: A multi-center study. Psychiatry and Clinical Neurosciences, 51, 275–279.
Ozaki, S., Uchiyama, M., Shirakawa, S., & Okawa, M. (1996). Prolonged interval from body temperature nadir to sleep offset in patients with delayed sleep phase syndrome. Sleep, 19, 36–40.
Pallesen, S. (2002). Insomnia in the elderly. Epidemiology, psychological characteristics and treatment. Doktoravhandling. Bergen: Det Psykologiske Fakultet, Universitetet i Bergen.
Pallesen, S. (2003). Behandling av søvnlidelser. Tidsskrift for Norsk Psykologforening, 40, 89–91.
Pallesen, S., Skjerve, A., & Bjorvatn, B. (i trykk). Light therapy for sleep and sleep related disturbances. I F. Columbus (Ed.), Progress in sleep research. Hauppauge, NY: Nova Science Publishers.
Pelayo, R. P., Thorpy, M. J., & Glovinsky, P. (1988). Prevalence of delayed sleep phase syndrome among adolescents. Sleep Research, 17, 391.
Pollak, C. A. (2000). Delayed-sleep-phase syndrome and other circadian-rhythm sleep disorders. I A. Culerbras (Ed.), Sleep disorders and neurological disease (ss. 159–177). New York: Marcel Dekker.
Regestein, Q. R., & Monk, T. H. (1995). Delayed sleep phase syndrome: A review of its clinical aspects. American Journal of Psychiatry, 152, 602–608.
Regestein, Q. R., & Pavlova, M. (1995). Treatment of delayed sleep phase syndrome. General Hospital Psychiatry, 17, 335–345.
Rosenthal, N. E., & Joseph-Vanderpool, J. R., Levendosky, A. A., Johnston, S. H., Allen, R., Kelly, K. A., Souetre, E., Schultz, P. M., & Starz, K. E. (1990). Phase-shifting effects of bright morning light as treatment for delayed sleep syndrome. Sleep, 13, 354–361.
Schrader, H., Bovim, G., & Sand, T. (1993). The prevalence of delayed and advanced sleep phase syndromes. Journal of Sleep Research, 2, 51–55.
Sheldon, S. H., Spire, J. P., & Levy, H. B. (1992). Sleep wake schedule disorders. I S. H. Sheldon, J. P. Spire & H. B. Levy (Eds.), Pediatric sleep medicine (ss. 106–118). Philadelphia: Saunders. Stepanski, E. J., & Wyatt, J. K. (2003). Use of sleep hygiene in the treatment of insomnia. Sleep Medicine Reviews, 7, 215–225.
Stores, G. (2001). A clinical guide to sleep disorders in children and adolescents. Cambridge: Cambridge University Press.
Sørensen, E., & Ursin, R. (2001). Søvnvaner hos ungdom. Tidsskrift for Den norske lægeforening, 121, 331–333.
Terman, M., & J. S. Terman (2000). Light therapy. I M. H. Kryger, T. Roth, & W. C. Dement (Eds.), Principles and practice of sleep medicine (3rd. ed., ss. 1258–1274). Philadelphia: W. B. Saunders Company.
Uchiyama, M., Okawa, M., Shibui, K., Liu, X. C., Hayakawa, T., Kamei, Y., & Takahashi, K. (2000). Poor compensatory function for sleep loss as a pathogenic factor in patients with delayed sleep phase syndrome. Sleep, 23, 553–558.
Ursin, R. (1996). Søvn. En lærebok om søvnforstyrrelser og søvnsykdommer. Oslo: Cappelen Akademisk Forlag.
Van den Hoofdakker, R. H. (1994). Chronobiological theories of nonseasonal affective disorders and their implications for treatment. Journal of Biological Rhythms, 9, 157–183.
von Gall, C., Stehle, J. H., & Weaver, D. R. (2002). Mammalian melatonin receptors: Molecular biology and signal transduction. Cell Tissue Research, 309, 151–162.
Weitzman, E. D., Czeisler, C. A., Coleman, R. M., Spielman, A. J., Zimmerman, J. C., Dement, W., Richardson, G., & Pollak, C. P. (1981). Delayed sleep phase syndrome. A chronobiological disorder with sleep-onset insomnia. Archives of General Psychiatry, 38, 737–746.
Whyte, J., & Schaefer, C. (1995). Introduction to sleep and its disorders. I C. E. Schaefer (Ed.), Clinical handbook of sleep disorders in children (ss. 1–14). Northvale, NJ: Jason Aronson.
World Health Organization. (1992). The ICD-10 classification of mental and behavioural disorders. Geneve: Author.
Yang, C. M., Spielman, A. J., D’Ambrosio, P., Serizawa, S., Nunes, J., & Birnbaum, J. (2001). A single dose of melatonin prevents the phase delay associated with a delayed weekend sleep pattern. Sleep, 24, 272–281.
Yazaki, M., Shirakawa, S., Okawa, M., & Takahashi, K. (1999). Demography of sleep disturbances associated with circadian rhythm disorders in Japan. Psychiatry and Clinical Neurosciences, 53, 267–268.
Zammit, G. K. (1997). Delayed sleep phase syndrome and related conditions. I M. R. Pressman & W. C. Orr (Eds.), Understanding sleep. The evaluation and treatment of sleep disorders (ss. 229–248). Washington, DC: American Psychological Association.
Zarcone, V. P. (1994). Seep hygiene. I H. Kryger, T. Roth, & W. C. Dement (Eds.), Principles and practice of sleep medicine (2nd ed. ss. 490–493). Philadelphia: W. B. Saunders Company.
